¿Qué significa diabetes tipo 1? Diabetes mellitus: síntomas, primeros signos, causas, tratamiento, nutrición y complicaciones de la diabetes. Lo que es
La diabetes mellitus es un importante problema médico y social en todo el mundo. Esto se explica por su amplia distribución, la gravedad de las complicaciones tardías y el alto coste de las herramientas de diagnóstico y tratamiento que los pacientes necesitan a lo largo de su vida.
Según los expertos de la Organización Mundial de la Salud, el número total de pacientes con todas las formas de diabetes mellitus hoy supera los 160 millones de personas. Cada año, el número de nuevos casos diagnosticados representa entre el 6 y el 10% del número total de pacientes, por lo que el número de personas que padecen esta enfermedad se duplica cada 10 a 15 años. La diabetes tipo 1 es la forma más grave de diabetes y representa no más del 10% de todos los casos de la enfermedad. La incidencia más alta se observa en niños de 10 a 15 años: 40,0 casos por 100 mil personas.
Un comité internacional de expertos, fundado en 1995 con el apoyo de la Asociación Estadounidense de Diabetes, propuso una nueva clasificación, que es aceptada en la mayoría de los países del mundo como documento de recomendación. La idea principal que subyace a la clasificación moderna de la diabetes es una identificación clara del factor etiológico en el desarrollo de la diabetes.
La diabetes mellitus tipo 1 es una enfermedad metabólica (metabólica) caracterizada por hiperglucemia, que se basa en la destrucción de las células β, lo que conduce a una deficiencia absoluta de insulina. Esta forma de diabetes se denominaba anteriormente diabetes mellitus insulinodependiente o diabetes mellitus juvenil. La destrucción de las células β en la mayoría de los casos entre la población europea es de naturaleza autoinmune (con la participación de los componentes celulares y humorales del sistema inmunológico) y es causada por la ausencia congénita o pérdida de tolerancia a los autoantígenos de las células β.
Múltiples factores genéticos predisponentes conducen a la destrucción autoinmune de las células β. La enfermedad tiene una clara asociación con el sistema HLA, con los genes DQ A1 y DQ B1, así como con DR B1. Los alelos HLA DR/DQ pueden ser tanto predisponentes como protectores.
La diabetes tipo 1 a menudo se combina con otras enfermedades autoinmunes, como la enfermedad de Graves (bocio tóxico difuso), la tiroiditis autoinmune, la enfermedad de Addison, el vitíligo y la anemia pernicítica. La diabetes tipo 1 puede ser un componente de un complejo de síndrome autoinmune (síndrome poliglandular autoinmune tipo 1 o 2, síndrome de “persona rígida”).
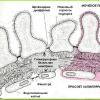
Resumiendo los datos clínicos y experimentales obtenidos hasta la fecha, podemos presentar el siguiente concepto de patogénesis de la diabetes tipo 1. A pesar de que parece tener un inicio agudo, la diabetes tipo 1 se desarrolla gradualmente. El período latente puede durar varios años. Los síntomas clínicos aparecen sólo después de que se ha destruido el 80% de las células β. Un estudio de autopsia del tejido pancreático de pacientes con diabetes tipo 1 revela el fenómeno de la insulitis, una inflamación específica caracterizada por la infiltración de islotes con linfocitos y monocitos.
Las primeras etapas del período preclínico de la diabetes tipo 1 se caracterizan por la aparición de clones de linfocitos T autorreactivos que producen citocinas, lo que conduce a la destrucción de las células β. Actualmente, la insulina, la glutamato descarboxilasa, la proteína de choque térmico 60 y la fogrina se consideran autoantígenos primarios putativos que, en determinadas condiciones, provocan la proliferación de linfocitos T citotóxicos.
En respuesta a la destrucción de las células β, las células plasmáticas secretan autoanticuerpos contra varios antígenos de las células β, que no participan directamente en la reacción autoinmune, pero indican la presencia de un proceso autoinmune. Estos autoanticuerpos pertenecen a la clase de las inmunoglobulinas G y se consideran marcadores inmunológicos de daño autoinmune a las células β. Hay autoanticuerpos contra células de los islotes (ICA, un conjunto de autoanticuerpos contra varios antígenos citoplasmáticos de las células β), autoanticuerpos específicos de las células β contra la insulina, anticuerpos contra la glutamato descarboxilasa (GAD), contra la fosfotirosina fosfatasa (IA-2) y fogrín. Los autoanticuerpos contra los antígenos de las células β son los marcadores más importantes de la destrucción autoinmune de las células β y aparecen en la diabetes tipo 1 típica mucho antes de que se desarrolle el cuadro clínico de la diabetes. Los autoanticuerpos contra las células de los islotes aparecen en el suero de 5 a 12 años antes de las primeras manifestaciones clínicas de diabetes mellitus, su título aumenta en la última etapa del período preclínico.
Hay 6 etapas en el desarrollo de la diabetes tipo 1, que comienzan con la predisposición genética y terminan con la destrucción completa de las células β.
La etapa 1 (predisposición genética) se caracteriza por la presencia o ausencia de genes asociados con la diabetes tipo 1. La primera etapa ocurre en menos de la mitad de los gemelos genéticamente idénticos y en el 2-5% de los hermanos. De gran importancia es la presencia de antígenos HLA, especialmente de clase II: DR 3, DR 4 y DQ.
Etapa 2: el comienzo del proceso autoinmune. Los factores externos que pueden desempeñar el papel de desencadenante en el desarrollo de daño autoinmune a las células β pueden ser: virus (virus Coxsackie B, rubéola, paperas, citomegalovirus, virus de Epstein-Barr), medicamentos, factores de estrés, factores nutricionales (uso de preparados para lactantes que contengan proteínas animales; productos que contengan nitrosaminas). El hecho de la exposición a diversos factores ambientales se puede establecer en el 60% de los pacientes con diabetes tipo 1 recién diagnosticada.
Etapa 3: desarrollo de trastornos inmunológicos. En la sangre se pueden detectar autoanticuerpos específicos contra diversas estructuras de células β: autoanticuerpos contra la insulina (IAA), ICA, GAD, IA2 e IA2b. En el estadio 3 se produce una alteración de la función de las células β y, como resultado de una disminución de la masa de las células β, una pérdida de la primera fase de la secreción de insulina, que puede diagnosticarse mediante la realización de una prueba de tolerancia a la glucosa intravenosa.
La etapa 4 (trastornos inmunológicos graves) se caracteriza por una intolerancia a la glucosa, pero no hay signos clínicos de diabetes mellitus. Al realizar una prueba de tolerancia oral a la glucosa (OGTT) se detecta un aumento de los niveles de glucosa en ayunas y/o 2 horas después de la OGTT.
En la etapa 5, se observa la manifestación clínica de la enfermedad, ya que en este momento muere la mayor parte de las células β (más del 80%). La baja secreción residual de péptido C persiste durante muchos años y es el factor más importante para mantener la homeostasis metabólica. Las manifestaciones clínicas de la enfermedad reflejan el grado de deficiencia de insulina.
La etapa 6 se caracteriza por una pérdida completa de la actividad funcional de las células β y una disminución de su número. Esta etapa se diagnostica cuando hay un nivel alto de glucemia, un nivel bajo de péptido C y no hay respuesta durante la prueba de esfuerzo. Esta etapa se llama diabetes “total”. Debido a la destrucción final de las células β en esta etapa, a veces se observa una disminución en el título de anticuerpos contra las células de los islotes o su desaparición completa.
También existe la diabetes mellitus idiopática tipo 1, en la que hay una disminución de la función de las células β con el desarrollo de síntomas de insulinopenia, como cetosis y cetoacidosis, pero no existen marcadores inmunológicos de destrucción autoinmune de las células β. Este subtipo de diabetes mellitus se presenta principalmente entre pacientes de raza africana o asiática. Esta forma de diabetes mellitus tiene una clara herencia. La necesidad absoluta de terapia de reemplazo en estos pacientes puede aparecer y desaparecer con el tiempo.
Como han demostrado los estudios de población, la diabetes tipo 1 entre la población adulta es mucho más común de lo que se pensaba anteriormente. En el 60% de los casos, la diabetes tipo 1 se desarrolla después de los 20 años. La aparición de diabetes en adultos puede tener un cuadro clínico diferente. La literatura describe el desarrollo asintomático de diabetes tipo 1 en familiares de primer y segundo grado de pacientes con diabetes tipo 1 con un título positivo de autoanticuerpos contra antígenos de células β, cuando el diagnóstico de diabetes mellitus se realizó únicamente con base en los resultados de una prueba de tolerancia oral a la glucosa.
El curso clásico de la diabetes tipo 1 con el desarrollo de un estado de cetoacidosis al inicio de la enfermedad también ocurre en adultos. El desarrollo de diabetes tipo 1 se ha descrito en todos los grupos de edad, hasta la novena década de la vida.
En casos típicos, la aparición de diabetes tipo 1 tiene síntomas clínicos pronunciados, que reflejan una deficiencia de insulina en el cuerpo. Los principales síntomas clínicos son: sequedad de boca, sed, micción frecuente, pérdida de peso. Muy a menudo, el inicio de la enfermedad es tan agudo que los pacientes pueden identificar el mes, y a veces incluso el día, en que experimentaron los síntomas mencionados por primera vez. La pérdida rápida de peso corporal, a veces de hasta 10-15 kg por mes, sin motivo aparente, es también uno de los principales síntomas de la diabetes tipo 1. En algunos casos, la aparición de la enfermedad va precedida de una infección viral grave (gripe, paperas, etc.) o estrés. Los pacientes se quejan de debilidad y fatiga severas. La diabetes mellitus autoinmune suele comenzar en niños y adolescentes, pero puede desarrollarse a cualquier edad.
Si hay síntomas de diabetes mellitus, son necesarias pruebas de laboratorio para confirmar el diagnóstico clínico. Los principales signos bioquímicos de la diabetes tipo 1 son: hiperglucemia (como regla general, se determina un alto porcentaje de azúcar en la sangre), glucosuria, cetonuria (la presencia de acetona en la orina). En casos graves, la descompensación del metabolismo de los carbohidratos conduce al desarrollo de coma cetoacidótico diabético.
Criterios diagnósticos de diabetes mellitus:
- glucosa plasmática en ayunas superior a 7,0 mmol/l (126 mg%);
- glucosa en sangre capilar en ayunas superior a 6,1 mmol/l (110 mg%);
- Glucosa plasmática (sangre capilar) 2 horas después de una comida (o una carga de 75 g de glucosa) superior a 11,1 mmol/l (200 mg%).
La determinación del nivel de péptido C en suero permite evaluar el estado funcional de las células β y, en casos dudosos, distinguir la diabetes tipo 1 de la diabetes tipo 2. Medir los niveles de péptido C es más informativo que los niveles de insulina. En algunos pacientes, al inicio de la diabetes tipo 1, se puede observar un nivel basal normal de péptido C, pero no hay aumento durante las pruebas de estimulación, lo que confirma la capacidad secretora insuficiente de las células β. Los principales marcadores que confirman la destrucción autoinmune de las células β son los autoanticuerpos contra los antígenos de las células β: autoanticuerpos contra GAD, ICA, insulina. Los autoanticuerpos contra las células de los islotes están presentes en el suero del 80-95% de los pacientes con diabetes tipo 1 recién diagnosticada y en el 60-87% de los individuos en el período preclínico de la enfermedad.
La progresión de la destrucción de las células β en la diabetes mellitus autoinmune (diabetes tipo 1) puede variar.
En la infancia, la pérdida de células β se produce rápidamente y al final del primer año de la enfermedad la función residual desaparece. En niños y adolescentes, la manifestación clínica de la enfermedad suele cursar con síntomas de cetoacidosis. Sin embargo, en los adultos también existe una forma lentamente progresiva de diabetes mellitus tipo 1, descrita en la literatura como diabetes autoinmune de adultos lentamente progresiva: diabetes autoinmune latente en adultos (LADA).
Diabetes autoinmune del adulto lentamente progresiva (LADA)
Esta es una variante especial del desarrollo de diabetes mellitus tipo 1 que se observa en adultos. El cuadro clínico de la diabetes tipo 2 y LADA al inicio de la enfermedad es similar: la compensación del metabolismo de los carbohidratos se logra mediante la dieta y/o el uso de hipoglucemiantes orales, pero luego, durante un período que puede durar de 6 meses a 6 años, se observa una descompensación del metabolismo de los carbohidratos y se desarrolla la necesidad de insulina. Un examen completo de estos pacientes revela marcadores genéticos e inmunológicos característicos de la diabetes tipo 1.
LADA se caracteriza por las siguientes características:
- edad de debut, generalmente superior a los 25 años;
- cuadro clínico de diabetes tipo 2 sin obesidad;
- inicialmente, control metabólico satisfactorio logrado mediante el uso de dieta y fármacos hipoglucemiantes orales;
- desarrollo de las necesidades de insulina en el período de 6 meses a 10 años (en promedio de 6 meses a 6 años);
- presencia de marcadores de diabetes tipo 1: nivel bajo de péptido C; la presencia de autoanticuerpos contra antígenos de células β (ICA y/o GAD); presencia de alelos HLA con alto riesgo de desarrollar diabetes tipo 1.
Como regla general, los pacientes con LADA no tienen un cuadro clínico claro de la aparición de diabetes tipo I, que es típica de niños y adolescentes. Al principio, LADA está “enmascarada” y se clasifica inicialmente como diabetes tipo 2 porque el proceso de destrucción autoinmune de las células β en adultos puede ser más lento que en niños. Los síntomas de la enfermedad se borran, no hay polidipsia pronunciada, poliuria, pérdida de peso ni cetoacidosis. El exceso de peso corporal tampoco excluye la posibilidad de desarrollar LADA. La función de las células β disminuye lentamente, a veces durante varios años, lo que previene el desarrollo de cetoacidosis y explica la compensación satisfactoria del metabolismo de los carbohidratos cuando se toma PSSP en los primeros años de la enfermedad. En tales casos, se diagnostica erróneamente diabetes tipo 2. La naturaleza gradual del desarrollo de la enfermedad conduce al hecho de que los pacientes buscan ayuda médica demasiado tarde, logrando adaptarse a la descompensación en desarrollo del metabolismo de los carbohidratos. En algunos casos, los pacientes acuden al médico entre 1 y 1,5 años después de la manifestación de la enfermedad. En este caso, se revelan todos los signos de una deficiencia aguda de insulina: bajo peso corporal, glucemia alta, falta de efecto del PSSP. P. Z. Zimmet (1999) dio la siguiente definición a este subtipo de diabetes tipo 1: “La diabetes autoinmune que se desarrolla en adultos puede no ser clínicamente diferente de la diabetes tipo 2 y se manifiesta por un lento deterioro del control metabólico con el posterior desarrollo de insulina. dependencia." Al mismo tiempo, la presencia en pacientes de los principales marcadores inmunológicos de la diabetes tipo 1: autoanticuerpos contra antígenos de células β, junto con niveles bajos de péptido C basal y estimulado, permite diagnosticar una diabetes autoinmune de progresión lenta en adultos.
Principales criterios diagnósticos de LADA:
- presencia de autoanticuerpos contra GAD y/o ICA;
- niveles bajos de péptido C basal y estimulado;
- Presencia de alelos HLA de alto riesgo para diabetes tipo 1.
La presencia de autoanticuerpos contra antígenos de células β en pacientes con síntomas clínicos de diabetes tipo II al inicio de la enfermedad tiene un alto valor pronóstico con respecto al desarrollo de la necesidad de insulina. Los resultados del Estudio Prospectivo de Diabetes del Reino Unido (UKPDS), que examinó a 3672 pacientes con un diagnóstico inicial de diabetes tipo 2, mostraron que los anticuerpos contra ICA y GAD tienen el mayor valor pronóstico en pacientes jóvenes ( ).
Según P. Zimmet, la prevalencia de LADA es de aproximadamente el 10-15% entre todos los pacientes con diabetes mellitus y aproximadamente el 50% de los casos ocurren en diabetes tipo 2 sin obesidad.
Los resultados de nuestro estudio mostraron que los pacientes de 30 a 64 años, que al inicio de la enfermedad presentaban un cuadro clínico de diabetes tipo 2 sin obesidad, disminución significativa del peso corporal (15,5 ± 9,1 kg) y enfermedades tiroideas autoinmunes concomitantes ( TDD) o AIT) representan un grupo con mayor riesgo de desarrollar LADA. La determinación de autoanticuerpos contra GAD, ICA e insulina en esta categoría de pacientes es necesaria para el diagnóstico oportuno de LADA. Con mayor frecuencia en LADA se detectan anticuerpos contra GAD (según nuestros datos, en el 65,1% de los pacientes con LADA), en comparación con los anticuerpos contra ICA (en el 23,3% de los LADA) y contra la insulina (en el 4,6% de los pacientes). La presencia de una combinación de anticuerpos no es típica. El título de anticuerpos contra GAD en pacientes con LADA es menor que en pacientes con diabetes tipo 1 con la misma duración de la enfermedad.
Los pacientes con LADA representan un grupo de alto riesgo de desarrollar necesidades de insulina y requieren la administración oportuna de terapia con insulina. Los resultados de OGTT indican la ausencia de secreción de insulina estimulada en el 46% de los pacientes con LADA y su disminución en el 30,7% de los pacientes ya en los primeros 5 años de la enfermedad. Como resultado de nuestro estudio, el 41,9% de los pacientes con LADA, cuya duración de la enfermedad no superaba los 5 años, cambiaron a insulina en una media de 25,2±20,1 meses desde el inicio de la enfermedad. Esta cifra fue significativamente mayor que en el grupo de pacientes con diabetes tipo 2 con la misma duración de la enfermedad (14% después de 24±21,07 meses desde el inicio de la enfermedad, p< 0,05).
Sin embargo, los pacientes con LADA representan un grupo heterogéneo de pacientes. El 53,7% de los pacientes con LADA tienen resistencia periférica a la insulina, mientras que el 30,7% de los pacientes tienen una combinación de resistencia a la insulina y deficiencia de insulina debido al daño autoinmune de las células β.
Al elegir tácticas de tratamiento en pacientes con LADA, se debe evaluar la secreción de insulina y la sensibilidad del tejido periférico a la insulina. Un nivel basal de péptido C inferior a 1 ng/ml (determinado mediante radioinmunoensayo) indica deficiencia de insulina. Sin embargo, para los pacientes con LADA, la ausencia de secreción de insulina estimulada es más típica, mientras que los valores de insulina en ayunas y de péptido C están dentro de los límites normales (cerca del límite inferior de lo normal). La relación entre la concentración máxima de insulina (en el minuto 90 de la prueba OGTT) y la inicial es inferior a 2,8 con valores iniciales bajos (4,6±0,6 µU/ml), lo que indica una secreción insuficiente de insulina estimulada e indica la necesidad. para la administración temprana de insulina.
La ausencia de obesidad, la descompensación del metabolismo de los carbohidratos al tomar PSSP, los niveles basales bajos de insulina y péptido C en pacientes con LADA indican una alta probabilidad de ausencia de secreción de insulina estimulada y la necesidad de administración de insulina.
Si los pacientes con LADA tienen un alto grado de resistencia a la insulina e hipersecreción de insulina en los primeros años de la enfermedad, se recomienda prescribir medicamentos que no agoten la función de las células β, pero que mejoren la sensibilidad periférica de los tejidos a la insulina, por ejemplo. ejemplo biguanidas o glitazonas (actos, avandia). Estos pacientes suelen tener sobrepeso y una compensación satisfactoria del metabolismo de los carbohidratos, pero requieren mayor observación. Para evaluar la resistencia a la insulina periférica, se puede utilizar el índice de resistencia a la insulina - Homa-IR = ins0/22,5 eLnglu0 (donde ins0 es el nivel de insulina en ayunas y glu0 es la glucosa plasmática en ayunas) y/o el índice de sensibilidad tisular general a la insulina (ISI - índice de sensibilidad a la insulina o índice de Matsuda ), obtenido en base a los resultados de la OGTT. Con tolerancia normal a la glucosa, Homa-IR es de 1,21 a 1,45 puntos; en pacientes con diabetes tipo 2, el valor de Homa-IR aumenta a 6 e incluso 12 puntos. El índice de Matsuda en el grupo con tolerancia normal a la glucosa es 7,3±0,1 UL -1 x ml x mg -1 x ml, y en presencia de resistencia a la insulina sus valores disminuyen.
Preservar la propia secreción de insulina residual en pacientes con diabetes mellitus tipo 1 es muy importante, ya que se observa que en estos casos la enfermedad es más estable y las complicaciones crónicas se desarrollan más lentamente y más tarde. Se discute la importancia del péptido C en el desarrollo de complicaciones tardías de la diabetes mellitus. En el experimento se descubrió que el péptido C mejora la función renal y la utilización de la glucosa. Se descubrió que la infusión de pequeñas dosis de péptido C biosintético puede afectar la microcirculación en el tejido muscular humano y la función renal.
Para determinar LADA, están indicados estudios inmunológicos más extendidos entre pacientes con diabetes tipo 1, especialmente en ausencia de obesidad e ineficacia temprana del PSSP. El principal método de diagnóstico es la determinación de autoanticuerpos contra GAD y ICA.
Un grupo especial de pacientes que también requieren mucha atención y en los que es necesario determinar autoanticuerpos contra GAD e ICA son las mujeres con diabetes mellitus gestacional (DMG). Se ha establecido que el 2% de las mujeres con diabetes mellitus gestacional desarrollan diabetes tipo 1 en un plazo de 15 años. Los mecanismos etiopatogenéticos del desarrollo de la DMG son muy heterogéneos, y para el médico siempre surge un dilema: ¿es la DMG la manifestación inicial de la diabetes tipo 1 o tipo 2? McEvoy et al. publicaron datos sobre la alta incidencia de autoanticuerpos contra ICA entre mujeres nativas y afroamericanas en Estados Unidos. Según otros datos, la prevalencia de autoanticuerpos contra ICA y GAD fue del 2,9 y el 5%, respectivamente, entre las mujeres finlandesas con antecedentes de DMG. Por tanto, los pacientes con DMG pueden experimentar un desarrollo lento de diabetes mellitus insulinodependiente, como ocurre con la diabetes LADA. El cribado de pacientes con DMG para determinar autoanticuerpos contra GAD e ICA permite identificar pacientes que requieren administración de insulina, lo que permitirá lograr una compensación óptima del metabolismo de los carbohidratos.
Teniendo en cuenta los mecanismos etiopatogenéticos del desarrollo de LADA, resulta obvio la necesidad de terapia con insulina en estos pacientes, mientras que la terapia temprana con insulina tiene como objetivo no solo compensar el metabolismo de los carbohidratos, sino que también permite mantener la secreción de insulina basal en un nivel satisfactorio durante un período prolongado. El uso de derivados de sulfonilurea en pacientes con LADA implica una mayor carga sobre las células β y su agotamiento más rápido, mientras que el tratamiento debe tener como objetivo mantener la secreción de insulina residual y atenuar la destrucción autoinmune de las células β. En este sentido, el uso de secretogenos en pacientes con LADA es patogenéticamente injustificado.
Después de la manifestación clínica, la mayoría de los pacientes con un cuadro clínico típico de diabetes tipo 1 experimentan en un período de 1 a 6 meses una disminución transitoria de las necesidades de insulina asociada con una mejora en la función de las células β restantes. Este es el período de remisión clínica de la enfermedad, o “luna de miel”. La necesidad de insulina exógena se reduce significativamente (menos de 0,4 unidades/kg de peso corporal, en casos raros, incluso es posible una retirada completa de la insulina); El desarrollo de la remisión es una característica distintiva del inicio de la diabetes tipo 1 y ocurre en el 18-62% de los casos de diabetes tipo 1 recién diagnosticada. La duración de la remisión varía de varios meses a 3-4 años.
A medida que avanza la enfermedad, la necesidad de insulina administrada de forma exógena aumenta y promedia 0,7-0,8 U/kg de peso corporal. Durante la pubertad, la necesidad de insulina puede aumentar significativamente, hasta 1,0-2,0 U/kg de peso corporal. Con el aumento de la duración de la enfermedad debido a la hiperglucemia crónica, se desarrollan complicaciones micro (retinopatía, nefropatía, polineuropatía) y macrovasculares de la diabetes mellitus (daño a los vasos coronarios, cerebrales y periféricos). La principal causa de muerte es la insuficiencia renal y las complicaciones de la aterosclerosis.
Tratamiento de la diabetes tipo 1
El objetivo del tratamiento para la diabetes tipo 1 es alcanzar los niveles objetivo de glucemia, presión arterial y lípidos en sangre ( ), que puede reducir significativamente el riesgo de desarrollar complicaciones micro y marcovasculares y mejorar la calidad de vida de los pacientes.
Los resultados del ensayo multicéntrico aleatorizado Diabetes Control and Complication Trail (DCCT) han demostrado de manera convincente que un buen control glucémico reduce la incidencia de complicaciones de la diabetes. Así, una disminución de la glucohemoglobina (HbA1c) del 9 al 7% condujo a una reducción del riesgo de desarrollar retinopatía diabética en un 76%, neuropatía en un 60% y microalbuminuria en un 54%.
El tratamiento de la diabetes tipo 1 incluye tres componentes principales:
- dietoterapia;
- ejercicio físico;
- terapia con insulina;
- entrenamiento y autocontrol.
Dietoterapia y actividad física.
En el tratamiento de la diabetes tipo 1, se deben excluir de la dieta diaria los alimentos que contengan carbohidratos de fácil digestión (azúcar, miel, dulces, bebidas dulces, mermeladas). Es necesario controlar el consumo (contar unidades de pan) de los siguientes productos: cereales, patatas, maíz, lácteos líquidos, frutas. La ingesta calórica diaria debe cubrirse en un 55-60% con carbohidratos, un 15-20% con proteínas y un 20-25% con grasas, mientras que la proporción de ácidos grasos saturados no debe superar el 10%.
El régimen de actividad física debe ser puramente individual. Cabe recordar que el ejercicio físico aumenta la sensibilidad de los tejidos a la insulina, reduce los niveles de glucemia y puede provocar el desarrollo de hipoglucemia. El riesgo de hipoglucemia aumenta durante la actividad física y durante 12 a 40 horas después de una actividad física intensa y prolongada. El ejercicio de ligero a moderado que no dure más de 1 hora requiere una ingesta adicional de carbohidratos de fácil digestión antes y después del ejercicio. Con actividad física moderada, prolongada (más de 1 hora) e intensa, es necesario ajustar las dosis de insulina. Es necesario medir los niveles de glucosa en sangre antes, durante y después del ejercicio.
La terapia de reemplazo de insulina de por vida es esencial para la supervivencia de los pacientes con diabetes tipo 1 y desempeña un papel crucial en el tratamiento rutinario de esta enfermedad. Al prescribir insulina, se pueden utilizar diferentes regímenes. Actualmente, se acostumbra distinguir entre regímenes de terapia con insulina tradicional e intensificada.
La característica principal del régimen tradicional de terapia con insulina es la falta de ajuste flexible de la dosis de insulina administrada al nivel glucémico. En este caso, el autocontrol de la glucosa en sangre suele estar ausente.
Los resultados del DCCT multicéntrico demostraron de manera convincente la ventaja de la terapia intensificada con insulina para compensar el metabolismo de los carbohidratos en la diabetes tipo 1. La terapia intensiva con insulina incluye lo siguiente:
- principio de bolo basal de la terapia con insulina (inyecciones múltiples);
- número previsto de unidades de pan para cada comida (liberalización de la dieta);
- autocontrol (control de la glucosa en sangre durante todo el día).
Para el tratamiento de la diabetes tipo 1 y la prevención de complicaciones vasculares, los fármacos de elección son las insulinas humanas genéticamente modificadas. Las insulinas semisintéticas porcinas y humanas obtenidas de la carne de cerdo son de menor calidad en comparación con las humanas genéticamente modificadas.
La terapia con insulina en esta etapa implica el uso de insulinas con diferentes duraciones de acción. Para crear un nivel básico de insulina, se utilizan insulinas de acción intermedia o de acción prolongada (aproximadamente 1 unidad por hora, que es un promedio de 24 a 26 unidades por día). Para regular el nivel de glucemia después de las comidas, se utilizan insulinas de acción corta o ultracorta en una dosis de 1-2 unidades por 1 unidad de pan ( ).
Las insulinas de acción ultracorta (humalog, novorapid), así como las insulinas de acción prolongada (lantus), son análogos de la insulina. Los análogos de la insulina son polipéptidos especialmente sintetizados que tienen la actividad biológica de la insulina y una serie de propiedades específicas. Estos son los preparados de insulina más prometedores en términos de terapia intensificada con insulina. Los análogos de la insulina Humalog (lispro, Lilly), así como novorapid (aspart, Novo Nordisk) son muy eficaces para regular la glucemia posprandial. Su uso también reduce el riesgo de hipoglucemia entre comidas. Lantus (insulina glargina, Aventis) se produce mediante tecnología de ADN recombinante utilizando una cepa de laboratorio no patógena de Escherichia coli (K12) como organismo productor y se diferencia de la insulina humana en que el aminoácido asparagina de la posición A21 se reemplaza por glicina y 2 Se añaden moléculas de arginina en el extremo C de la cadena B. Estos cambios permitieron obtener un perfil de concentración constante y libre de picos de acción de la insulina durante las 24 horas del día.
Se han creado mezclas preparadas de insulinas humanas de diversas acciones, como Mixtard (30/70), Insuman Comb (25/75, 30/70), etc., que son mezclas estables de insulina de acción corta y prolongada. en proporciones especificadas.
Para la administración de insulina se utilizan jeringas de insulina desechables (U-100 para administrar insulina con una concentración de 100 U/ml y U-40 para insulina con una concentración de 40 U/ml), plumas de jeringa (Novopen, Humapen, Optipen, Bd -pen, Plivapen) y bombas de insulina. Se deben proporcionar jeringas a todos los niños y adolescentes con diabetes tipo 1, así como a las mujeres embarazadas con diabetes, a los pacientes con problemas de visión y a los amputados de miembros inferiores debido a la diabetes.
Alcanzar los valores glucémicos objetivo es imposible sin un autocontrol regular y un ajuste de las dosis de insulina. Los pacientes con diabetes tipo 1 deben controlar de forma independiente la glucemia diariamente, varias veces al día, para lo cual no solo se pueden usar glucómetros, sino también tiras reactivas para la determinación visual del azúcar en sangre (Glucocromo D, Betachek, Suprima Plus).
Para reducir la incidencia de complicaciones micro y macrovasculares de la diabetes, es importante alcanzar y mantener niveles normales de metabolismo de los lípidos y presión arterial.
El nivel objetivo de presión arterial para la diabetes tipo 1 en ausencia de proteinuria es la PA.< 135/85 мм рт. ст., а при наличии протеинурии — более 1 г/сут и при хронической почечной недостаточности — АД < 125/75 мм рт. ст.
El desarrollo y progresión de las enfermedades cardiovasculares depende en gran medida del nivel de lípidos en sangre. Así, con niveles de colesterol superiores a 6,0 mol/l, LDL > 4,0 mmol/l, HDL< 1,0 ммоль/ и триглицеридах выше 2,2 ммоль/л у больных СД 1 типа наблюдается высокий риск развития сердечно-сосудистых осложнений. Терапевтическими целями лечения, определяющими низкий риск развития сердечно-сосудистых осложнений у больных СД 1 типа, являются: общий холестерин < 4,8 ммоль/л, ЛПНП < 3,0 ммоль/л, ЛПВП >1,2 mmol/l, triglicéridos< 1,7 ммоль/л.
En las próximas décadas, continuarán las investigaciones para crear nuevas formas farmacéuticas de insulina y medios de administración que permitan que la terapia de reemplazo se acerque lo más posible a la naturaleza fisiológica de la secreción de insulina. Se están realizando investigaciones sobre el trasplante de células de los islotes. Sin embargo, una alternativa real al alotrasplante o xenotrasplante de cultivos o células de los islotes "frescas" es el desarrollo de métodos biotecnológicos: terapia génica, generación de células β a partir de células madre, diferenciación de células secretoras de insulina de células del conducto pancreático o células pancreáticas. . Sin embargo, hoy en día la insulina sigue siendo el principal tratamiento para la diabetes.
Si tiene preguntas sobre la literatura, comuníquese con el editor.
I. V. Kononenko, Candidato de Ciencias Médicas
O. M. Smirnova,Doctor en Ciencias Médicas, Profesor
Centro de Investigaciones Endocrinológicas de la Academia Rusa de Ciencias Médicas, Moscú
En el mundo moderno, la diabetes mellitus es una de las enfermedades que se clasifica como un problema médico y social grave a escala mundial, ya que tiene una alta prevalencia, complicaciones graves y además requiere importantes costos financieros para procedimientos diagnósticos y terapéuticos, que Será necesario para el enfermo toda su vida. Es por ello que muchos esfuerzos y recursos en todo el sector sanitario se destinan a un estudio más profundo de las causas y mecanismos del desarrollo de la diabetes mellitus, así como a encontrar nuevos métodos eficaces para prevenirla y combatirla.
¿Qué es la diabetes tipo 1?
La diabetes mellitus es una enfermedad crónica, cuyo rasgo característico es una violación de los procesos metabólicos, acompañada de hiperglucemia (aumento de los niveles de glucosa en sangre), que surge como resultado de una violación de la producción de insulina por parte de la glándula endocrina (páncreas). o una violación de su acción. Las estadísticas muestran que el número total de personas con diabetes mellitus de todas las formas en el mundo supera actualmente los 160 millones de personas. Se registran nuevos casos de morbilidad con tanta frecuencia que el número de pacientes se duplica cada década. La forma más grave de diabetes mellitus en términos de corrección y posibles complicaciones se considera la diabetes mellitus tipo 1, cuya incidencia oscila entre el 8 y el 10% de todos los casos de la enfermedad.
Diabetes mellitus tipo 1 - una enfermedad del sistema endocrino, cuyo rasgo característico es un aumento de la concentración de glucosa en la sangre, que se desarrolla debido a procesos destructivos en células específicas del páncreas que secretan la hormona insulina, lo que resulta en una falta absoluta de insulina en el cuerpo. Se observa una alta incidencia de diabetes tipo 1 en niños de la adolescencia y la edad adulta temprana: 40 casos por 100.000 personas. Anteriormente, esta forma de diabetes se llamaba diabetes juvenil y dependiente de insulina.
Hay dos formas de diabetes mellitus tipo 1: autoinmune e idiopático.
Causas que contribuyen al desarrollo de diabetes mellitus tipo 1.
Desarrollo forma autoinmune de diabetes mellitus tipo 1 La mayoría de las veces comienza en la infancia, pero también se puede diagnosticar en personas mayores. En este caso, se detectan autoanticuerpos (anticuerpos producidos contra los propios antígenos del cuerpo humano) contra los componentes estructurales de las células β, células pancreáticas específicas que producen insulina, es decir, contra sus antígenos de superficie, insulina, glutamato descarboxilasa, etc. Se forman debido a una pérdida congénita o adquirida de tolerancia (insensibilidad) a los autoantígenos.células β. Como resultado de este proceso, se desarrolla la destrucción autoinmune de las células β. En los niños, el proceso de descomposición de estas células es rápido, por lo que ya un año después del inicio del proceso patológico, la secreción de insulina en el páncreas se detiene por completo. En el cuerpo de los adultos, el proceso de destrucción celular lleva más tiempo, por lo que las células β pueden secretar cantidades suficientes de insulina durante un largo período de tiempo, lo que puede prevenir el desarrollo de complicaciones de la diabetes como la cetoacidosis. Sin embargo, una disminución en la secreción de insulina es inevitable y, después de un cierto tiempo, se desarrolla su deficiencia absoluta.
Predispone a la degradación autoinmunecélulas pancreáticas que producen insulina y una serie de factores genéticos. La diabetes mellitus tipo 1 a menudo se diagnostica en combinación con enfermedades autoinmunes como el bocio tóxico difuso, la tiroiditis autoinmune, la enfermedad de Addison, el vitiligo y el complejo de síndrome autoinmune.
Forma idiopática de diabetes mellitus tipo 1. es bastante raro. En este caso, los pacientes no tienen factores inmunológicos y genéticos para la diabetes mellitus tipo 1, pero existen síntomas que confirman la deficiencia absoluta de insulina.
El curso de la diabetes mellitus tipo 1.
La diabetes tipo 1 se caracteriza por un período de latencia, cuya duración puede oscilar entre un año y varios años. El desarrollo de la enfermedad pasa por varias etapas:
Nivel 1.Presencia de predisposición genética. Si se detectan antígenos específicos del sistema en la sangre. HLA , entonces la probabilidad de desarrollar diabetes tipo 1 aumenta significativamente.
Etapa 2.Sospecha de factor desencadenante. Pueden ser agentes de naturaleza infecciosa: enterovirus, retrovirus, togavirus, así como causas no infecciosas: dieta, estrés psicoemocional, exposición a sustancias químicas, toxinas y venenos, insolación (irradiación solar), radiación, etc.
Etapa 3.Hay trastornos del sistema inmunológico: la aparición de autoanticuerpos contra antígenos.Células β, insulina, tirosina fosfatasa, con niveles normales de insulina en la sangre. En este caso, la primera fase de producción de insulina está ausente.
Etapa 4.Se caracteriza por alteraciones inmunitarias graves, es decir, la secreción de insulina disminuye rápidamente debido al desarrollo de insulitis (inflamación de los islotes de Langerhans del páncreas, que contienen células que producen insulina), se altera la resistencia a la glucosa, mientras que los niveles de azúcar en sangre se mantienen dentro de los límites normales. límites.
Etapa 5.Se caracteriza por manifestaciones clínicas pronunciadas, ya que tres cuartas partesEn este punto las células β se destruyen. Sólo se conserva la secreción residual de péptido C.
Etapa 6.Muerte total de las células β. No se detecta péptido C, los títulos de anticuerpos disminuyen. Esta etapa también se llama diabetes total. El curso de la diabetes mellitus se vuelve incontrolable, lo que amenaza con el desarrollo de complicaciones graves: coagulación intravascular diseminada, edema de la corteza cerebral y el desarrollo de coma diabético.
¿Cómo se manifiesta la diabetes tipo 1?
Dado que los signos clínicos aparecen cuando se destruyen la mayoría de las células β del páncreas, el inicio de la enfermedad es siempre agudo y puede aparecer por primera vez acidosis severa o coma diabetico. En niños y adolescentes, la aparición de la enfermedad se caracteriza por signos de cetoacidosis. A veces, los pacientes pueden nombrar claramente el día en que notaron los signos de la enfermedad. A veces, la aparición de la enfermedad puede ir precedida de una infección viral grave (influenza, paperas, rubéola).
Los pacientes pueden quejarse de sequedad de boca y sensación de sed causada por la excreción excesiva de líquido del cuerpo por los riñones, micción frecuente, aumento del apetito junto con una impresionante pérdida de peso corporal (hasta 10-15 kg por mes), debilidad general. y fatiga. Además, los pacientes pueden quejarse de picazón, procesos pustosos en la piel y las uñas y visión borrosa. En el aspecto sexual, los pacientes notan una disminución del deseo y la potencia sexual. En la cavidad bucal se pueden detectar signos de enfermedad periodontal, piorrea alveolar, gingivitis y estomatitis. Lesiones cariosas de los dientes.
Al examinar a pacientes con diabetes tipo 1, se detecta un aumento en la concentración de azúcar en sangre y su presencia en la orina. En la etapa de descompensación, los expertos notan sequedad de la piel de los pacientes, sus membranas mucosas, lengua, disminución de la turgencia de la grasa subcutánea, enrojecimiento de las mejillas, la frente y el mentón debido a la dilatación de los capilares cutáneos de la cara. Si el proceso de descompensación se prolonga, los pacientes pueden desarrollar complicaciones como oftalmopatía diabética, nefropatía, neuropatía periférica, osteoartropatía diabética, etc. Las niñas pueden desarrollar infertilidad y los niños pueden experimentar un deterioro y retraso notable en el crecimiento y el desarrollo físico.
Criterios diagnósticos de diabetes mellitus tipo 1.
Si, junto con los signos clínicos, se produce un aumento de la concentración de glucosa en sangre (más de 11,1 mmol/l) en cualquier momento del día, entonces podemos hablar de diabetes mellitus.
Los expertos de la Organización Mundial de la Salud han desarrollado una serie de criterios que se utilizan para diagnosticar la diabetes mellitus. En primer lugar, se trata de determinar el nivel de glucosa en sangre en ayunas, es decir, cuando han pasado al menos 8 horas desde la última comida. También es necesario determinar el nivel de glucosa en sangre de forma aleatoria, es decir, en cualquier momento dentro de las 24 horas, independientemente del momento en que se consuman los alimentos.
Para valorar en qué etapa de la diabetes se encuentra el paciente son necesarias las siguientes pruebas de laboratorio:
Análisis general de orina y sangre;
La concentración de glucosa en sangre con el estómago vacío y luego un par de horas después de comer;
Determinación del nivel de hemoglobina glicosilada;
Nivel de cuerpos cetónicos y glucosa en la orina diaria;
Química de la sangre;
Análisis de orina según Nechiporenko.
Para el diagnóstico diferencial de la diabetes mellitus tipo 1, se realiza un análisis del contenido de marcadores inmunológicos y genéticos y del nivel de péptido C.
Además, los pacientes se someten a una serie de estudios instrumentales obligatorios: electrocardiografía, radiografía de tórax y oftalmoscopia.
A pesar de que el cuadro clínico de la diabetes mellitus insulinodependiente y no insulinodependiente tiene muchas similitudes, el diagnóstico diferencial entre ellas se basa en una serie de diferencias. Si la diabetes mellitus tipo 1 se caracteriza por una disminución del peso corporal de los pacientes, la diabetes mellitus tipo 2 se caracteriza por un aumento de peso. La diabetes mellitus tipo 1 comienza de forma aguda, a diferencia de la diabetes mellitus tipo 2, que se caracteriza por un lento aumento de los síntomas. La diabetes mellitus tipo 2 se diagnostica con mayor frecuencia en adultos y personas mayores (mayores de 45 años), y la diabetes mellitus tipo 1 se diagnostica con mayor frecuencia en niños y jóvenes. En estudios de laboratorio, los anticuerpos contra los antígenos de las células β se detectan solo en la diabetes insulinodependiente.
Si a un paciente se le diagnostica diabetes tipo 1 por primera vez, debe ser hospitalizado para seleccionar un régimen de tratamiento con insulina, aprender a controlar de forma independiente los niveles de glucosa en sangre, desarrollar una dieta y un régimen de trabajo. Además, están sujetos a hospitalización los pacientes en estado precomatoso y comatoso, con cetoacidosis diabética, con aumento de la angiopatía, con el agregado de infecciones, así como si es necesaria alguna intervención quirúrgica.
Tratamiento de la diabetes tipo 1
El objetivo principal del tratamiento de pacientes con diabetes tipo 1 es preservar su vida, así como mejorar su calidad. Para ello, se toman medidas preventivas para prevenir el desarrollo de complicaciones agudas y crónicas y la corrección de patologías concomitantes.
El tratamiento de la diabetes mellitus tipo 1 implica un conjunto de medidas, incluida la terapia con insulina, que actualmente el único método para corregir la deficiencia absoluta de insulina. Para estos fines, nuestro país utiliza análogos de la insulina humana o la insulina obtenida mediante ingeniería genética. La terapia sustitutiva con insulina se puede realizar según el régimen tradicional, cuando se administra un determinado nivel de insulina por vía subcutánea sin adaptar constantemente la dosis al nivel de glucemia. La terapia intensiva con insulina tiene grandes ventajas, que incluyen múltiples inyecciones de insulina, corrección de la dieta contando unidades de pan y control de los niveles de glucosa a lo largo del día.
El siguiente punto en el régimen de tratamiento de la diabetes es el desarrollo de un programa de nutrición especial que normalizará el peso corporal y ayudará a mantener los niveles de glucosa en sangre dentro de los límites normales. Los alimentos para pacientes con diabetes deben ser bajos en calorías, no contener carbohidratos refinados (dulces, bebidas dulces, mermeladas) y respetar estrictamente los horarios de las comidas. Es necesario excluir de la dieta los alimentos enlatados, las carnes ahumadas y los alimentos ricos en grasas (crema agria, mayonesa, nueces). La proporción de los principales componentes energéticos de la dieta suele equipararse a la fisiológica y es de 3:1:1.
La actividad física de los pacientes con diabetes tipo 1 debe ser moderada y seleccionarse individualmente, según la gravedad de la enfermedad. La mejor forma de actividad física es caminar. Sin embargo, debe recordarse que los zapatos deben seleccionarse de tal manera que eviten la formación de callos y callosidades, que pueden convertirse en el comienzo de una complicación peligrosa de la diabetes: el pie diabético.
El resultado del tratamiento de la diabetes está directamente relacionado con la participación activa del propio paciente, quien debe ser capacitado por personal médico en métodos de autocontrol de los niveles de glucosa en sangre mediante glucómetros y tiras reactivas, ya que necesita realizar esta manipulación al menos. 3-4 veces al día. Además, el paciente debe evaluar su estado, controlar su dieta y cantidad de actividad física, así como visitar periódicamente al médico tratante, quien, además de hablar con el paciente, debe examinarle las piernas y medir la presión arterial. Una vez al año, un paciente con diabetes tipo 1 debe someterse a todas las pruebas necesarias (análisis bioquímico de sangre, análisis general de sangre y orina, determinación del nivel de hemoglobina glicosilada), someterse a un examen por parte de un oftalmólogo y un neurólogo y realizarse un examen de tórax. -rayo.
Prevenir el desarrollo de diabetes mellitus tipo 1
El desarrollo de diabetes mellitus tipo 1 en personas con alta predisposición genética se puede prevenir previniendo infecciones virales intrauterinas, así como contrayendo infecciones virales en la infancia y la adolescencia. No se deben incluir en la dieta de los niños predispuestos a la enfermedad, fórmulas nutricionales que contengan gluten, alimentos con conservantes y colorantes que puedan provocar una reacción autoinmune contra las células del páncreas productoras de insulina.
Complicaciones de la diabetes
La razón principal del desarrollo de complicaciones de la diabetes mellitus es el daño vascular debido a la descompensación prolongada de la diabetes mellitus (hiperglucemia prolongada - niveles altos de azúcar en sangre). En primer lugar, la microcirculación se ve afectada, es decir, se altera el suministro de sangre a los vasos más pequeños.
Tratamiento de la diabetes
La diabetes mellitus es un grupo de enfermedades metabólicas caracterizadas por niveles elevados de glucosa (“azúcar”) en la sangre.
Tipos de diabetes
Actualmente, existen dos tipos principales de diabetes mellitus, que se diferencian en la causa y el mecanismo de aparición, así como en los principios de tratamiento.
Dieta para la diabetes
Numerosos estudios en todo el mundo se centran en encontrar tratamientos eficaces para la diabetes. Sin embargo, no debemos olvidar que, además de la terapia farmacológica, no son menos importantes las recomendaciones de cambios en el estilo de vida.
Diabetes mellitus gestacional durante el embarazo.
La diabetes mellitus gestacional puede desarrollarse durante el embarazo (en aproximadamente el 4% de los casos). Se basa en una disminución de la capacidad de absorber glucosa.
hipoglucemia
La hipoglucemia es una condición patológica caracterizada por una disminución de la concentración de glucosa plasmática por debajo de 2,8 mmol/l, que se presenta con ciertos síntomas clínicos, o menos de 2,2 mmol/l, independientemente de la presencia o ausencia de signos clínicos.
Coma con diabetes mellitus
La información sobre la complicación más peligrosa de la diabetes mellitus, que requiere atención médica de emergencia, es el coma. Se describen los tipos de coma en la diabetes mellitus, sus síntomas específicos y tácticas de tratamiento.
Síndrome poliglandular autoinmune
El síndrome poliglandular autoinmune es un grupo de endocrinopatías que se caracterizan por la participación de varias glándulas endocrinas en el proceso patológico como resultado de su daño autoinmune.
El síndrome del pie diabético es una de las complicaciones de la diabetes mellitus, junto con la oftalmopatía diabética, nefropatía, etc., que es una condición patológica resultante del daño al sistema nervioso periférico, arterial y microvasculatura, que se manifiesta por procesos purulentos-necróticos, ulcerativos y daño. a los huesos y articulaciones del pie
Acerca de la diabetes
Diabetes mellitus es un término que une las enfermedades endocrinas, cuyo rasgo característico es la insuficiencia de la acción de la hormona insulina. El síntoma principal de la diabetes mellitus es el desarrollo de hiperglucemia, un aumento persistente de la concentración de glucosa en la sangre.
Síntomas de diabetes
La eficacia del tratamiento de la diabetes depende directamente del momento de detección de esta enfermedad. En la diabetes mellitus tipo 2, la enfermedad puede provocar durante mucho tiempo sólo molestias leves a las que el paciente puede no prestar atención. Los síntomas de la diabetes pueden ser sutiles, lo que dificulta el diagnóstico. Cuanto antes se haga el diagnóstico correcto y se inicie el tratamiento, menor será el riesgo de desarrollar complicaciones de la diabetes.
Muy a menudo, los pacientes menores de 18 años acuden a los especialistas del Centro de Endocrinología del Noroeste. Para ellos, el centro cuenta con médicos especiales: endocrinólogos pediátricos.
La diabetes mellitus tipo 1 es una enfermedad endocrina autoinmune, cuyo principal criterio diagnóstico es la hiperglucemia crónica, debida a una falta absoluta de producción de insulina por parte de las células beta del páncreas.
La insulina es una hormona proteica que ayuda a que la glucosa pase de la sangre a las células. Sin él, la glucosa no se absorbe y permanece en la sangre en alta concentración. Un nivel alto de glucosa en la sangre no proporciona valor energético y, con una hiperglucemia prolongada, comienza el daño a los vasos sanguíneos y las fibras nerviosas. Al mismo tiempo, las células están "privadas" de energía, no tienen suficiente glucosa para llevar a cabo procesos metabólicos, luego comienzan a extraer energía de las grasas y luego de las proteínas. Todo esto conlleva muchas consecuencias, que comentaremos a continuación.
El término "glucemia" significa nivel de azúcar en sangre.
La hiperglucemia son niveles elevados de azúcar en sangre.
Hipoglucemia: el nivel de azúcar en sangre está por debajo de lo normal.
Un glucómetro es un dispositivo para determinar de forma independiente el azúcar en sangre capilar. Se extrae sangre con un escarificador (agujas desechables incluidas en el kit), se aplica una gota de sangre a una tira reactiva y se inserta en el dispositivo. En la pantalla se muestran números que reflejan el nivel actual de azúcar en sangre.
Causas de la diabetes tipo 1
Las razones son genéticas y la predisposición hereditaria es de primordial importancia.
Clasificación de la diabetes mellitus tipo 1
1. Por compensación
La diabetes compensada es un estado de diabetes en el que los niveles de metabolismo de los carbohidratos son cercanos a los de una persona sana.
Subcompensación. Puede haber episodios de corta duración de hiperglucemia o hipoglucemia, sin deterioro significativo de las funciones vitales.
Descompensación. El azúcar en sangre fluctúa ampliamente, con estados hipoglucémicos e hiperglucémicos, hasta el desarrollo de precoma y coma. Aparece acetona (cuerpos cetónicos) en la orina.
2. Según la presencia de complicaciones
Sin complicaciones (diabetes de curso inicial o idealmente compensada, que no presenta complicaciones, que se describen a continuación);
- complicado (hay complicaciones vasculares y/o neuropatías)
3. Por origen
Autoinmune (se han detectado anticuerpos contra las propias células);
- idiopático (la causa no ha sido identificada).
Esta clasificación sólo tiene importancia científica, ya que no influye en las tácticas de tratamiento.
Síntomas de la diabetes tipo 1:
1. Sed (con niveles elevados de azúcar en sangre, el cuerpo requiere “dilución” de la sangre, reduciendo la glucemia, esto se logra bebiendo mucho líquido, esto se llama polidipsia).
2. Micción abundante y frecuente, micción nocturna (la ingesta de grandes cantidades de líquido, así como los niveles altos de glucosa en la orina, contribuyen a la micción en volúmenes grandes e inusuales, esto se llama poliuria).
3. Aumento del apetito (no olvide que las células del cuerpo se mueren de hambre y, por tanto, señalan sus necesidades).
4. Pérdida de peso (las células, al no recibir carbohidratos para obtener energía, comienzan a alimentarse de grasas y proteínas, respectivamente, no queda material para la construcción y renovación de los tejidos, una persona pierde peso con mayor apetito y sed).
5. La piel y las membranas mucosas están secas y, a menudo, hay quejas de que la boca "se seca".
6. Estado general con rendimiento reducido, debilidad, fatiga, dolores musculares y dolores de cabeza (también debido a la falta de energía de todas las células).
7. Ataques de sudoración, picor de la piel (en las mujeres, el picor en el perineo suele ser el primero en aparecer).
8. Baja resistencia a las infecciones (exacerbación de enfermedades crónicas, como amigdalitis crónica, aparición de aftas, susceptibilidad a infecciones virales agudas).
9. Náuseas, vómitos, dolor abdominal en la región epigástrica (debajo del estómago).
10. A largo plazo, la aparición de complicaciones: disminución de la visión, alteración de la función renal, alteración de la nutrición y suministro de sangre a las extremidades inferiores, alteración de la inervación motora y sensorial de las extremidades, así como la formación de polineuropatía autonómica.
Diagnóstico:

Angiopatía en diabetes
Como ya se mencionó, una alta concentración de glucosa en sangre daña la pared vascular, lo que conduce al desarrollo de microangiopatía (daño a los vasos pequeños) y macroangiopatía (daño a los vasos grandes).
A las microangiopatías incluyen: retinopatía retiniana (daño a los pequeños vasos de los ojos), nefropatía (daño al aparato vascular de los riñones) y lesiones de pequeños vasos de otros órganos. Los signos clínicos de microangiopatía aparecen aproximadamente entre los 10 y 15 años de diabetes tipo 1, pero puede haber desviaciones de las estadísticas. Si la diabetes está bien compensada y se realiza un tratamiento adicional de manera oportuna, entonces el desarrollo de esta complicación puede "posponerse" indefinidamente. También hay casos de desarrollo muy temprano de microangiopatía, ya 2 o 3 años después del inicio de la enfermedad.
En los pacientes jóvenes, el daño vascular es "puramente diabético" y en las generaciones mayores se combina con la aterosclerosis vascular, lo que empeora el pronóstico y el curso de la enfermedad.
Morfológicamente, la microangiopatía es una lesión múltiple de pequeños vasos en todos los órganos y tejidos. La pared vascular se espesa y aparecen en ella depósitos hialinos (sustancia proteica de alta densidad y resistente a diversas influencias). Debido a esto, los vasos pierden su permeabilidad y flexibilidad normales, los nutrientes y el oxígeno tienen dificultades para penetrar en los tejidos, los tejidos se agotan y sufren falta de oxígeno y nutrición. Además, los vasos afectados se vuelven más vulnerables y frágiles. Como ya se ha dicho, muchos órganos se ven afectados, pero el más significativo clínicamente es el daño a los riñones y la retina.
Prevención de la diabetes tipo 1
En el caso de la diabetes mellitus tipo 1, la tarea del paciente es prevenir complicaciones. Esto le ayudará a consultar periódicamente con un endocrinólogo, así como a participar en escuelas de diabetes. La Escuela de Diabetes es una actividad de sensibilización realizada por médicos de diversas especialidades. Los endocrinólogos, cirujanos y terapeutas enseñan a los pacientes a contar unidades de pan, autocontrolar el nivel de azúcar en la sangre, reconocer condiciones que empeoran y brindarse asistencia propia y mutua, cuidar sus pies (esto es extremadamente importante en el desarrollo de la angiopatía y la neuropatía) y otras habilidades útiles. .
La diabetes tipo 1 es una enfermedad que se convierte en una forma de vida. Cambia su rutina habitual, pero no interfiere con su éxito ni con sus planes de vida. No está limitado en sus actividades profesionales, libertad de movimiento y deseo de tener hijos. Muchas personas famosas viven con diabetes, entre ellas Sharon Stone, Halle Berry, el jugador de hockey Bobby Clarke y muchos otros. La clave del éxito es el autocontrol y la consulta oportuna con un médico. ¡Cuídate y mantente saludable!
Médico general Petrova A.V.
La diabetes mellitus es actualmente una de las enfermedades más comunes, principalmente debido a que afecta cada vez a más personas jóvenes. Sin embargo, existe la diabetes tipo 1 que se manifiesta en pacientes menores de 30 años, provocando ciertos síntomas y requiriendo insulina.
Actualmente se conocen con precisión las causas de la diabetes tipo 1. Las tendencias genéticas son, en cierta medida, responsables de su aparición. Especialmente cuando los parientes cercanos tienen diabetes. No necesariamente será del mismo tipo; a menudo, la enfermedad en sí se hereda y se manifiesta de diversas formas.
La diabetes tipo 1 es causada principalmente por infecciones pasadas, en su mayoría virales. Cuando ocurren o como resultado de un tratamiento inadecuado, se produce daño en las células pancreáticas llamadas islotes de Langerhans o células beta. Como resultado, la glándula comienza a funcionar mal, interrumpiendo la producción de insulina.
Este tipo de diabetes durante mucho tiempo se llamó diabetes juvenil, porque. la mayoría de las enfermedades ocurren entre los 20 y 30 años de edad. Los primeros síntomas pueden aparecer al comienzo de la adolescencia, así como antes de los 18 años; esto es casi la mitad del número de casos diagnosticados.
La diabetes mellitus tipo 1 es una enfermedad de los jóvenes, también llamada diabetes juvenil. Las personas menores de 35 años son susceptibles a la enfermedad. Hay causas de diabetes juvenil 1a, presumiblemente de naturaleza viral, que aparecen solo en la infancia, y causas de diabetes juvenil 1b (la más común): se detectan anticuerpos contra las células de insulina, hay una disminución o cese de la producción de insulina por parte de las páncreas. Este tipo representa entre el 1,5% y el 2% de todos los casos de diabetes.
La diabetes juvenil es una enfermedad con predisposición hereditaria, pero la contribución del genotipo al desarrollo de la enfermedad es pequeña. Ocurre en niños con una madre enferma con una probabilidad de 1-2%, padre - 3-6%, hermano o hermana - 6%. Tener diabetes tipo 2 en familiares de primer grado también aumenta el riesgo de desarrollar diabetes tipo 1.
Si una persona con predisposición hereditaria ingresa un virus al cuerpo, la enfermedad infecciosa provocará el desarrollo de anticuerpos contra las células beta. Como resultado, las células que producen insulina morirán. Pero lo "insidioso" de la diabetes es que los signos de la enfermedad no aparecen de inmediato: primero es necesario destruir más del 80% de las células β, lo que puede ocurrir en varios meses o varios años. Como resultado, muchos pacientes experimentan inmediatamente una deficiencia absoluta de insulina.
Como regla general, la enfermedad se desarrolla según el siguiente escenario:
- La presencia de una predisposición genética a la diabetes.
- Destrucción de las células β (células de los islotes de Langerhans) del páncreas. La muerte celular puede ser de naturaleza autoinmune o comenzar bajo la influencia de factores ambientales, por ejemplo, después de que una infección viral ingresa al cuerpo. Dichos agentes pueden ser el citomegalovirus, la rubéola, el sarampión, el virus Coxsackie B, la varicela y los virus de las paperas. También se conocen sustancias tóxicas que afectan selectivamente a las células beta e inducen una reacción autoinmune.
- Estrés psicoemocional. Hay casos de diabetes de aparición repentina después de un estrés intenso. Las situaciones estresantes provocan la exacerbación de diversas enfermedades crónicas y los efectos de los virus.
- Una reacción inflamatoria en los islotes pancreáticos llamada "insulitis".
- Transformación de las células β por parte del sistema inmunológico porque se perciben como extrañas.
- Rechazo de los islotes pancreáticos, aparecen anticuerpos citotóxicos.
- Destrucción de células β y aparición de signos evidentes de diabetes.
La diabetes mellitus tipo 1 presenta síntomas graves y es bastante aguda, caracterizándose por un deterioro progresivo del estado del paciente en ausencia de tratamiento. Por lo general, los pacientes pueden nombrar con precisión el período de aparición de los primeros síntomas. Se caracteriza por sed, micción frecuente y copiosa, a veces más de 6 litros por día, sequedad de boca, debilidad general, fatiga, picazón en la piel, picazón en el perineo, hambre insaciable y pérdida de peso.
Los síntomas bastante comunes también son irritabilidad, dolor en el corazón, en los músculos de la pantorrilla, dolor de cabeza, etc. El examen revela azúcar en la orina, aumento de la glucosa en sangre y deficiencia de insulina. Además, el nivel de insulina en plasma puede ser tan bajo que ni siquiera sea detectable.
En la diabetes clínicamente significativa, la glucemia en ayunas es >120 mg/dL o >6,7 mmol/L, y la glucemia 2 horas después de una comida principal es >180 mg/dL o >10 mmol/L. Se produce un rápido deterioro de la salud y una deshidratación grave. Si los medicamentos de insulina no se prescriben a tiempo, el paciente puede desarrollar un coma diabético.
La enfermedad es peligrosa debido al desarrollo de complicaciones: accidente cerebrovascular, infarto, daño ocular hasta ceguera, con desarrollo de insuficiencia renal, con resultado de gangrena y pérdida de una extremidad, atrofia muscular, osteoporosis, etc.
La terapia con insulina es necesaria ante los primeros síntomas de la diabetes tipo 1. Vale la pena señalar que hay casos de normalización completa del metabolismo con la ayuda de preparaciones de insulina. Es decir, la diabetes mellitus tipo 1 puede remitir con la detección y administración oportuna de insulina. Sin embargo, incluso en tales casos, la recuperación completa es imposible.
Actualmente, la diabetes mellitus es una enfermedad incurable. El principal método de tratamiento es únicamente la inyección regular de insulina en el cuerpo. Si ya se ha desarrollado diabetes, entonces es imposible restaurar las células β. Están intentando trasplantar el páncreas y las células que producen insulina, pero hasta ahora sin éxito.
Desafortunadamente, todavía no existe una forma de insulina que no sea destruida por el jugo gástrico una vez que ingresa al estómago a través de la boca. Por tanto, la terapia con insulina se realiza mediante inyección o cosiendo una bomba de insulina. Además de las jeringas de insulina tradicionales, existen dispositivos de inyección estilo pluma que hacen que las inyecciones de insulina sean fáciles y convenientes.
En este caso, se utilizan los siguientes tipos de preparaciones de insulina:
- período de validez provisional
- Actuación rápida
- de larga duración
La elección del fármaco óptimo, así como la selección de la dosis y el número de inyecciones, debe realizarla un endocrinólogo.
La mayoría de los pacientes que reciben medicamentos con insulina controlan su afección mediante el autocontrol de sus niveles de azúcar en sangre. Esto es importante porque lo principal en el tratamiento de la diabetes tipo 1 es esforzarse por mantener concentraciones constantes de glucosa en sangre. Para mantener el nivel de glucemia en un cierto nivel, se deben seguir algunas reglas al seleccionar la dosis de insulina:
Es posible alcanzar la normoglucemia no sólo variando las dosis de insulina, sino también realizando un seguimiento constante de las calorías consumidas. En función de su peso corporal ideal, debe calcular su ingesta de proteínas, grasas y carbohidratos y crear una dieta equilibrada.
Existen ciertas reglas que debe seguir un paciente con este tipo de diabetes:
Quedan completamente excluidos el azúcar, las mermeladas, los dulces y otros carbohidratos de rápida absorción, ya que provocan un fuerte salto en los niveles de glucosa en sangre. Se recomienda consumirlos sólo durante un ataque de hipoglucemia, en combinación con carbohidratos "complejos" y fibra.
Los carbohidratos “complejos” se encuentran en los cereales, los frijoles, las patatas y otras verduras. Tardan más en digerirse, lo que resulta muy beneficioso para los pacientes con diabetes tipo 1. La inclusión suficiente de verduras, frutas y bayas en la dieta es beneficiosa, ya que contienen vitaminas y microelementos, son ricas en fibra dietética y garantizan un metabolismo normal en el cuerpo.
¡Atención!
Pero hay que tener en cuenta que algunas frutas y bayas (ciruelas pasas, fresas, etc.) contienen muchos carbohidratos, por lo que solo se pueden consumir teniendo en cuenta la cantidad diaria de carbohidratos en la dieta.
La industria alimentaria produce variedades especiales de pan, galletas, bizcochos y pasteles que contienen carbohidratos mucho menos digeribles de lo habitual. Para satisfacer las necesidades gustativas, y también en parte con fines medicinales, se recomienda la inclusión de diversos sucedáneos del azúcar.
El consumo de bebidas alcohólicas debe limitarse o suspenderse drásticamente, ya que el alcohol es una bebida rica en calorías y, además, tiene un efecto adverso sobre las funciones de todos los órganos y sistemas (principalmente el sistema nervioso).
Para normalizar los niveles de glucosa en sangre, es importante no solo seguir una dieta, sino también llevar un estilo de vida activo. Cualquier actividad física mejora la circulación sanguínea y reduce los niveles de azúcar en sangre:
- Durante el ejercicio, aumenta la sensibilidad de los tejidos corporales a la insulina y la velocidad de su absorción.
- El consumo de glucosa aumenta sin dosis adicionales de insulina.
- Con entrenamiento regular, la normoglucemia se estabiliza mucho más rápido.
El ejercicio físico afecta en gran medida al metabolismo de los carbohidratos, por lo que es importante recordar que durante el entrenamiento el cuerpo utiliza activamente las reservas de glucógeno, por lo que puede producirse hipoglucemia después del ejercicio. No puede hacer ejercicio si no se siente bien. Es importante llevar consigo carbohidratos "simples", por ejemplo, un par de dulces.
Para que las células musculares absorban la glucosa, debe haber suficiente insulina en la sangre. Debe comenzar a hacer ejercicio cuando su nivel de azúcar en sangre no sea inferior a 5 mmol/l ni superior a 15 mmol/l. Lo mejor es hacer ejercicio con un entrenador o con amigos que tengan conocimientos sobre el cuidado de la diabetes y la hipoglucemia.
La diabetes tipo 1 requiere ejercicio regular y dosificado. El ejercicio intenso y repentino provoca un desequilibrio en los niveles de glucosa en sangre. Una caminata rápida, trotar, realizar tareas domésticas activas o ir a una discoteca pueden considerarse actividad física. La actividad física ideal es caminar.
El modo óptimo de actividad física es hacer ejercicio 5 veces por semana durante 30 minutos. La intensidad del ejercicio debe ser tal que la frecuencia cardíaca del paciente alcance hasta el 65% del máximo. La frecuencia cardíaca máxima se calcula individualmente mediante la fórmula: 220 menos la edad. Al caminar, no debe olvidarse de los requisitos para el calzado, que no debe dañar sus pies. Si tienes síndrome del pie diabético, debes prestar especial atención al cuidado de los pies después del ejercicio.
Fuente: http://insulat.ru/diabet/diabet_1_tipa
Diabetes mellitus tipo 1
En el mundo moderno, la diabetes mellitus es una de las enfermedades que se clasifica como un problema médico y social grave a escala mundial, ya que tiene una alta prevalencia, complicaciones graves y además requiere importantes costos financieros para procedimientos diagnósticos y terapéuticos, que Será necesario para el enfermo toda su vida.
Es por ello que muchos esfuerzos y recursos en todo el sector sanitario se dirigen a un estudio más profundo de las causas y mecanismos del desarrollo de la diabetes mellitus, así como a encontrar nuevos métodos eficaces para combatirla.
¿Qué es la diabetes tipo 1?
La diabetes mellitus es una enfermedad crónica, cuyo rasgo característico es una violación de los procesos metabólicos, acompañada de (aumento de los niveles de glucosa en sangre), que surge como resultado de una violación de la producción de insulina por parte de la glándula endocrina (páncreas), o una violación de su acción.
Las estadísticas muestran que el número total de personas con diabetes mellitus de todas las formas en el mundo supera actualmente los 160 millones de personas. Se registran nuevos casos de morbilidad con tanta frecuencia que el número de pacientes se duplica cada década. La forma más grave de diabetes mellitus en términos de corrección y posibles complicaciones se considera la diabetes mellitus tipo 1, cuya incidencia oscila entre el 8 y el 10% de todos los casos de la enfermedad.
La diabetes mellitus tipo 1 es una enfermedad del sistema endocrino, cuyo rasgo característico es un aumento de la concentración de glucosa en la sangre, que se desarrolla debido a procesos destructivos en células pancreáticas específicas que secretan la hormona insulina, lo que resulta en una falta absoluta de insulina. en el cuerpo. Se observa una alta incidencia de diabetes tipo 1 en niños de la adolescencia y la edad adulta temprana: 40 casos por 100.000 personas. Anteriormente, esta forma de diabetes se llamaba diabetes juvenil y dependiente de insulina.
Hay dos formas de diabetes tipo 1: autoinmune e idiopática.
Razones que promueven el desarrollo
El desarrollo de la forma autoinmune de diabetes mellitus tipo 1 comienza con mayor frecuencia en la infancia, pero también puede diagnosticarse en personas mayores. En este caso, se detectan autoanticuerpos (anticuerpos producidos contra los propios antígenos del cuerpo humano) contra los componentes estructurales de las células β, células pancreáticas específicas que producen insulina, es decir, contra sus antígenos de superficie, insulina, glutamato descarboxilasa, etc.
Se forman debido a una pérdida de tolerancia (insensibilidad) congénita o adquirida a los autoantígenos de las células β. Como resultado de este proceso, se desarrolla la destrucción autoinmune de las células β. En los niños, el proceso de descomposición de estas células es rápido, por lo que ya un año después del inicio del proceso patológico, la secreción de insulina en el páncreas se detiene por completo.
En el cuerpo de los adultos, el proceso de destrucción celular lleva más tiempo, por lo que las células β pueden secretar cantidades suficientes de insulina durante un largo período de tiempo, lo que puede prevenir el desarrollo de complicaciones de la diabetes como la cetoacidosis. Sin embargo, una disminución en la secreción de insulina es inevitable y, después de un cierto tiempo, se desarrolla su deficiencia absoluta.
Varios factores genéticos también predisponen a la destrucción autoinmune de las células pancreáticas que producen insulina. La diabetes mellitus tipo 1 a menudo se diagnostica en combinación con enfermedades autoinmunes como el bocio tóxico difuso, la tiroiditis autoinmune, la enfermedad de Addison, el vitiligo y el complejo de síndrome autoinmune.
La forma idiopática de diabetes mellitus tipo 1 es bastante rara. En este caso, los pacientes no tienen factores inmunológicos y genéticos para la diabetes mellitus tipo 1, pero existen síntomas que confirman la deficiencia absoluta de insulina.
Fluir
La diabetes tipo 1 se caracteriza por un período de latencia, cuya duración puede oscilar entre un año y varios años. El desarrollo de la enfermedad pasa por varias etapas:
- Nivel 1. Presencia de predisposición genética. Si se detectan antígenos específicos del sistema HLA en la sangre, la probabilidad de desarrollar diabetes tipo 1 aumenta significativamente.
- Etapa 2. Sospecha de factor desencadenante. Pueden ser agentes de naturaleza infecciosa: enterovirus, retrovirus, togavirus, así como causas no infecciosas: dieta, estrés psicoemocional, exposición a sustancias químicas, toxinas y venenos, insolación (irradiación solar), radiación, etc.
- Etapa 3. Hay trastornos del sistema inmunológico (la aparición de autoanticuerpos contra antígenos de células β, insulina, tirosina fosfatasa) con niveles normales de insulina en la sangre. En este caso, la primera fase de producción de insulina está ausente.
- Etapa 4. Se caracteriza por alteraciones inmunitarias graves, es decir, la secreción de insulina disminuye rápidamente debido al desarrollo de insulitis (inflamación de los islotes de Langerhans del páncreas, que contienen células que producen insulina), se altera la resistencia a la glucosa, mientras que los niveles de azúcar en sangre se mantienen dentro de los límites normales. límites.
- Etapa 5. Las manifestaciones clínicas pronunciadas son típicas, ya que en este punto tres cuartas partes de las células β están destruidas. Sólo se conserva la secreción residual de péptido C.
- Etapa 6. Muerte total de las células β. No se detecta péptido C, los títulos de anticuerpos disminuyen. Esta etapa también se llama diabetes total. El curso de la diabetes mellitus se vuelve incontrolable, lo que amenaza con el desarrollo de complicaciones graves: coagulación intravascular diseminada, edema de la corteza cerebral y el desarrollo de coma diabético.
¿Cómo se manifiesta?
Debido a que los signos clínicos aparecen cuando se destruye la mayoría de las células β pancreáticas, el inicio de la enfermedad siempre es agudo y puede manifestarse primero como acidosis grave o coma diabético. En niños y adolescentes, la aparición de la enfermedad se caracteriza por síntomas. A veces, los pacientes pueden nombrar claramente el día en que notaron los signos de la enfermedad. A veces, la aparición de la enfermedad puede ir precedida de una infección viral grave (influenza, paperas, rubéola).
Los pacientes pueden quejarse de sequedad de boca y sensación de sed causada por la excreción excesiva de líquido del cuerpo por los riñones, micción frecuente, aumento del apetito junto con una impresionante pérdida de peso corporal (hasta 10-15 kg por mes), debilidad general. y fatiga.
Además, los pacientes pueden quejarse de picazón, procesos pustosos en la piel y las uñas y visión borrosa. En el aspecto sexual, los pacientes notan una disminución del deseo y la potencia sexual. En la cavidad bucal se pueden detectar signos de enfermedad periodontal, piorrea alveolar, gingivitis y estomatitis. Lesiones cariosas de los dientes.
Al examinar a pacientes con diabetes tipo 1, se detecta un aumento en la concentración de azúcar en sangre y su presencia en la orina. En la etapa de descompensación, los expertos notan sequedad de la piel de los pacientes, sus membranas mucosas, lengua, disminución de la turgencia de la grasa subcutánea, enrojecimiento de las mejillas, la frente y el mentón debido a la dilatación de los capilares cutáneos de la cara.
Si el proceso de descompensación se prolonga, los pacientes pueden desarrollar complicaciones como oftalmopatía diabética, nefropatía, neuropatía periférica, osteoartropatía diabética, etc. Las niñas pueden desarrollar infertilidad y los niños pueden experimentar un deterioro y retraso notable en el crecimiento y el desarrollo físico.
Criterios de diagnóstico
Si, junto con los signos clínicos, se produce un aumento de la concentración de glucosa en sangre (más de 11,1 mmol/l) en cualquier momento del día, entonces podemos hablar de diabetes mellitus.
Los expertos de la Organización Mundial de la Salud han desarrollado una serie de criterios que se utilizan para diagnosticar la diabetes mellitus. En primer lugar, se trata de determinar el nivel de glucosa en sangre en ayunas, es decir, cuando han pasado al menos 8 horas desde la última comida. También es necesario determinar el nivel de glucosa en sangre de forma aleatoria, es decir, en cualquier momento dentro de las 24 horas, independientemente del momento en que se consuman los alimentos.
Para valorar en qué etapa de la diabetes se encuentra el paciente son necesarias las siguientes pruebas de laboratorio:
- análisis general de orina y sangre;
- la concentración de glucosa en sangre con el estómago vacío y luego un par de horas después de comer;
- determinación del nivel de hemoglobina glicosilada;
- nivel de cuerpos cetónicos y glucosa en la orina diaria;
- química de la sangre;
- análisis de orina según Nechiporenko.
Para el diagnóstico diferencial de la diabetes mellitus tipo 1, se realiza un análisis del contenido de marcadores inmunológicos y genéticos y del nivel de péptido C. Además, los pacientes se someten a una serie de estudios instrumentales obligatorios: electrocardiografía, radiografía de tórax y oftalmoscopia.
¡Atención!
A pesar de que el cuadro clínico de la diabetes mellitus insulinodependiente y no insulinodependiente tiene muchas similitudes, el diagnóstico diferencial entre ellas se basa en una serie de diferencias. Si la diabetes mellitus tipo 1 se caracteriza por una disminución del peso corporal de los pacientes, la diabetes mellitus tipo 2 se caracteriza por un aumento de peso.
La diabetes mellitus tipo 1 comienza de forma aguda, a diferencia de la diabetes mellitus tipo 2, que se caracteriza por un lento aumento de los síntomas. La diabetes mellitus tipo 2 se diagnostica con mayor frecuencia en adultos y personas mayores (mayores de 45 años), y la diabetes mellitus tipo 1 se diagnostica con mayor frecuencia en niños y jóvenes. En estudios de laboratorio, los anticuerpos contra los antígenos de las células β se detectan solo en la diabetes insulinodependiente.
Si a un paciente se le diagnostica diabetes tipo 1 por primera vez, debe ser hospitalizado para seleccionar un régimen de tratamiento con insulina, aprender a controlar de forma independiente los niveles de glucosa en sangre, desarrollar una dieta y un régimen de trabajo.
Además, están sujetos a hospitalización los pacientes en estado precomatoso y comatoso, con cetoacidosis diabética, con aumento de la angiopatía, con el agregado de infecciones, así como si es necesaria alguna intervención quirúrgica.
Tratamiento
El objetivo principal del tratamiento de pacientes con diabetes tipo 1 es preservar su vida, así como mejorar su calidad. Para ello, se toman medidas preventivas para prevenir el desarrollo de complicaciones agudas y crónicas y la corrección de patologías concomitantes.
El tratamiento de la diabetes mellitus tipo 1 implica un conjunto de medidas, que incluyen la terapia con insulina, que actualmente es el único método para corregir la deficiencia absoluta de insulina. Para estos fines, nuestro país utiliza análogos de la insulina humana o la insulina obtenida mediante ingeniería genética.
La terapia sustitutiva con insulina se puede realizar según el régimen tradicional, cuando se administra un determinado nivel de insulina por vía subcutánea sin adaptar constantemente la dosis al nivel de glucemia. La terapia intensiva con insulina tiene grandes ventajas, que incluyen múltiples inyecciones de insulina, corrección de la dieta contando unidades de pan y control de los niveles de glucosa a lo largo del día.
El siguiente punto en el régimen de tratamiento de la diabetes es el desarrollo de un programa de nutrición especial que normalizará el peso corporal y ayudará a mantener los niveles de glucosa en sangre dentro de los límites normales. Los alimentos para pacientes con diabetes deben ser bajos en calorías, no contener carbohidratos refinados (dulces, bebidas dulces, mermeladas) y respetar estrictamente los horarios de las comidas.
Es necesario excluir de la dieta los alimentos enlatados, las carnes ahumadas y los alimentos ricos en grasas (crema agria, mayonesa, nueces). La proporción de los principales componentes energéticos de la dieta suele equipararse a la fisiológica y es de 3:1:1.
La actividad física de los pacientes con diabetes tipo 1 debe ser moderada y seleccionarse individualmente, según la gravedad de la enfermedad. La mejor forma de actividad física es caminar. Sin embargo, debe recordarse que los zapatos deben seleccionarse de tal manera que eviten la formación de callos y callosidades, que pueden convertirse en el comienzo de una complicación peligrosa de la diabetes mellitus: el pie diabético.
El resultado del tratamiento de la diabetes está directamente relacionado con la participación activa del propio paciente, quien debe ser capacitado por personal médico en métodos de autocontrol de los niveles de glucosa en sangre mediante tiras reactivas, pues necesita realizar esta manipulación al menos 3- 4 veces al día.
Además, el paciente debe evaluar su estado, controlar su dieta y cantidad de actividad física, así como visitar periódicamente al médico tratante, quien, además de hablar con el paciente, debe examinarle las piernas y medir la presión arterial. Una vez al año, un paciente con diabetes tipo 1 debe someterse a todas las pruebas necesarias (análisis bioquímico de sangre, análisis general de sangre y orina, determinación del nivel de hemoglobina glicosilada), someterse a un examen por parte de un oftalmólogo y un neurólogo y realizarse un examen de tórax. -rayo.
Prevención del desarrollo
El desarrollo de diabetes mellitus tipo 1 en personas con alta predisposición genética se puede prevenir previniendo infecciones virales intrauterinas, así como contrayendo infecciones virales en la infancia y la adolescencia.
No se deben incluir en la dieta de los niños predispuestos a la enfermedad, fórmulas nutricionales que contengan gluten, alimentos con conservantes y colorantes que puedan provocar una reacción autoinmune contra las células del páncreas productoras de insulina.
Fuente: http://www.endoinfo.ru/theory_pacients/sakharnyy-diabet/sakharnyy-diabet-1-tipa.html
Diabetes mellitus tipo 1 en adultos
La diabetes mellitus es un importante problema médico y social en todo el mundo. Esto se explica por su amplia distribución, la gravedad de las complicaciones tardías y el alto coste de las herramientas de diagnóstico y tratamiento que los pacientes necesitan a lo largo de su vida.
Según los expertos de la Organización Mundial de la Salud, el número total de pacientes con todas las formas de diabetes mellitus hoy supera los 160 millones de personas. Cada año, el número de nuevos casos diagnosticados representa entre el 6 y el 10% del número total de pacientes, por lo que el número de personas que padecen esta enfermedad se duplica cada 10 a 15 años.
La diabetes tipo 1 es la forma más grave de diabetes y representa no más del 10% de todos los casos de la enfermedad. La incidencia más alta se observa en niños de 10 a 15 años: 40,0 casos por 100 mil personas.
Un comité internacional de expertos, fundado en 1995 con el apoyo de la Asociación Estadounidense de Diabetes, propuso una nueva clasificación, que es aceptada en la mayoría de los países del mundo como documento de recomendación. La idea principal que subyace a la clasificación moderna de la diabetes es una identificación clara del factor etiológico en el desarrollo de la diabetes.
La diabetes mellitus tipo 1 es una enfermedad metabólica (metabólica) caracterizada por hiperglucemia, que se basa en la destrucción de las células β, lo que conduce a una deficiencia absoluta de insulina. Esta forma de diabetes se denominaba anteriormente diabetes mellitus insulinodependiente o diabetes mellitus juvenil.
La destrucción de las células β en la mayoría de los casos entre la población europea es de naturaleza autoinmune (con la participación de los componentes celulares y humorales del sistema inmunológico) y es causada por la ausencia congénita o pérdida de tolerancia a los autoantígenos de las células β.
Múltiples factores genéticos predisponentes conducen a la destrucción autoinmune de las células β. La enfermedad tiene una clara asociación con el sistema HLA, con los genes DQ A1 y DQ B1, así como con DR B1. Los alelos HLA DR/DQ pueden ser tanto predisponentes como protectores.
La diabetes tipo 1 a menudo se combina con otras enfermedades autoinmunes, como la enfermedad de Graves (bocio tóxico difuso), la tiroiditis autoinmune, la enfermedad de Addison, el vitíligo y la anemia pernicítica. La diabetes tipo 1 puede ser un componente de un complejo de síndrome autoinmune (síndrome poliglandular autoinmune tipo 1 o 2, síndrome de “persona rígida”).
¡Atención!
Resumiendo los datos clínicos y experimentales obtenidos hasta la fecha, podemos presentar el siguiente concepto de patogénesis de la diabetes tipo 1. A pesar de que parece tener un inicio agudo, la diabetes tipo 1 se desarrolla gradualmente. El período latente puede durar varios años. Los síntomas clínicos aparecen sólo después de que se ha destruido el 80% de las células β.
Un estudio de autopsia del tejido pancreático de pacientes con diabetes tipo 1 revela el fenómeno de la insulitis, una inflamación específica caracterizada por la infiltración de islotes con linfocitos y monocitos.
Las primeras etapas del período preclínico de la diabetes tipo 1 se caracterizan por la aparición de clones de linfocitos T autorreactivos que producen citocinas, lo que conduce a la destrucción de las células β. Actualmente, la insulina, la glutamato descarboxilasa, la proteína de choque térmico 60 y la fogrina se consideran autoantígenos primarios putativos que, en determinadas condiciones, provocan la proliferación de linfocitos T citotóxicos.
En respuesta a la destrucción de las células β, las células plasmáticas secretan autoanticuerpos contra varios antígenos de las células β, que no participan directamente en la reacción autoinmune, pero indican la presencia de un proceso autoinmune. Estos autoanticuerpos pertenecen a la clase de las inmunoglobulinas G y se consideran marcadores inmunológicos de daño autoinmune a las células β.
Hay autoanticuerpos contra células de los islotes (ICA, un conjunto de autoanticuerpos contra varios antígenos citoplasmáticos de las células β), autoanticuerpos específicos de las células β contra la insulina, anticuerpos contra la glutamato descarboxilasa (GAD), contra la fosfotirosina fosfatasa (IA-2) y fogrín.
Los autoanticuerpos contra los antígenos de las células β son los marcadores más importantes de la destrucción autoinmune de las células β y aparecen en la diabetes tipo 1 típica mucho antes de que se desarrolle el cuadro clínico de la diabetes. Los autoanticuerpos contra las células de los islotes aparecen en el suero de 5 a 12 años antes de las primeras manifestaciones clínicas de diabetes mellitus y su título aumenta en la última etapa del período preclínico.
También existe la diabetes mellitus idiopática tipo 1, en la que hay una disminución de la función de las células β con el desarrollo de síntomas de insulinopenia, como cetosis y cetoacidosis, pero no existen marcadores inmunológicos de destrucción autoinmune de las células β. Este subtipo de diabetes mellitus se presenta principalmente entre pacientes de raza africana o asiática. Esta forma de diabetes mellitus tiene una clara herencia. La necesidad absoluta de terapia de reemplazo en estos pacientes puede aparecer y desaparecer con el tiempo.
Como han demostrado los estudios de población, la diabetes tipo 1 entre la población adulta es mucho más común de lo que se pensaba anteriormente. En el 60% de los casos, la diabetes tipo 1 se desarrolla después de los 20 años. La aparición de diabetes en adultos puede tener un cuadro clínico diferente. La literatura describe el desarrollo asintomático de diabetes tipo 1 en familiares de primer y segundo grado de pacientes con diabetes tipo 1 con un título positivo de autoanticuerpos contra antígenos de células β, cuando el diagnóstico de diabetes mellitus se realizó únicamente con base en los resultados de una prueba de tolerancia oral a la glucosa.
El curso clásico de la diabetes tipo 1 con el desarrollo de un estado de cetoacidosis al inicio de la enfermedad también ocurre en adultos. El desarrollo de diabetes tipo 1 se ha descrito en todos los grupos de edad, hasta la novena década de la vida.
En casos típicos, la aparición de diabetes tipo 1 tiene síntomas clínicos pronunciados, que reflejan una deficiencia de insulina en el cuerpo. Los principales síntomas clínicos son: sequedad de boca, sed, micción frecuente, pérdida de peso. Muy a menudo, el inicio de la enfermedad es tan agudo que los pacientes pueden identificar el mes, y a veces incluso el día, en que experimentaron los síntomas mencionados por primera vez.
La pérdida rápida de peso corporal, a veces de hasta 10 a 15 kg por mes, sin motivo aparente, es también uno de los principales síntomas de la diabetes tipo 1. En algunos casos, la aparición de la enfermedad va precedida de una infección viral grave (gripe, paperas, etc.) o estrés. Los pacientes se quejan de debilidad y fatiga severas. La diabetes mellitus autoinmune suele comenzar en niños y adolescentes, pero puede desarrollarse a cualquier edad.
Si hay síntomas de diabetes mellitus, son necesarias pruebas de laboratorio para confirmar el diagnóstico clínico. Los principales signos bioquímicos de la diabetes tipo 1 son: hiperglucemia (como regla general, se determina un alto porcentaje de azúcar en la sangre), glucosuria, cetonuria (la presencia de acetona en la orina). En casos graves, la descompensación del metabolismo de los carbohidratos conduce al desarrollo de coma cetoacidótico diabético.
Criterios diagnósticos de diabetes mellitus:
- glucosa plasmática en ayunas superior a 7,0 mmol/l (126 mg%);
- glucosa en sangre capilar en ayunas superior a 6,1 mmol/l (110 mg%);
- Glucosa plasmática (sangre capilar) 2 horas después de una comida (o una carga de 75 g de glucosa) superior a 11,1 mmol/l (200 mg%).
La determinación del nivel de péptido C en suero permite evaluar el estado funcional de las células β y, en casos dudosos, distinguir la diabetes tipo 1 de la diabetes tipo 2. Medir los niveles de péptido C es más informativo que los niveles de insulina. En algunos pacientes, al inicio de la diabetes tipo 1, se puede observar un nivel basal normal de péptido C, pero no hay aumento durante las pruebas de estimulación, lo que confirma la capacidad secretora insuficiente de las células β.
Los principales marcadores que confirman la destrucción autoinmune de las células β son los autoanticuerpos contra los antígenos de las células β: autoanticuerpos contra GAD, ICA, insulina. Los autoanticuerpos contra las células de los islotes están presentes en el suero de 80 a 95% de los pacientes con diabetes tipo 1 recién diagnosticada y en 60 a 87% de los individuos en el período preclínico de la enfermedad.
La progresión de la destrucción de las células β en la diabetes mellitus autoinmune (diabetes tipo 1) puede variar. En la infancia, la pérdida de células β se produce rápidamente y al final del primer año de la enfermedad la función residual desaparece. En niños y adolescentes, la manifestación clínica de la enfermedad suele cursar con síntomas de cetoacidosis. Sin embargo, en los adultos también existe una forma lentamente progresiva de diabetes mellitus tipo 1, descrita en la literatura como diabetes autoinmune de adultos lentamente progresiva: diabetes autoinmune latente en adultos (LADA).
Diabetes autoinmune del adulto lentamente progresiva (LADA)
Esta es una variante especial del desarrollo de diabetes mellitus tipo 1 que se observa en adultos. El cuadro clínico de la diabetes tipo 2 y LADA al inicio de la enfermedad es similar: la compensación del metabolismo de los carbohidratos se logra mediante la dieta y/o el uso de hipoglucemiantes orales, pero luego, durante un período que puede durar de 6 meses a 6 años, se observa una descompensación del metabolismo de los carbohidratos y se desarrolla la necesidad de insulina. Un examen completo de estos pacientes revela marcadores genéticos e inmunológicos característicos de la diabetes tipo 1.
LADA se caracteriza por las siguientes características:
- edad de debut, generalmente superior a los 25 años;
- cuadro clínico de diabetes tipo 2 sin obesidad;
- inicialmente, control metabólico satisfactorio logrado mediante el uso de dieta y fármacos hipoglucemiantes orales;
- desarrollo de las necesidades de insulina en el período de 6 meses a 10 años (en promedio de 6 meses a 6 años);
- presencia de marcadores de diabetes tipo 1: nivel bajo de péptido C; la presencia de autoanticuerpos contra antígenos de células β (ICA y/o GAD); presencia de alelos HLA con alto riesgo de desarrollar diabetes tipo 1.
Como regla general, los pacientes con LADA no tienen un cuadro clínico claro de la aparición de diabetes tipo I, que es típica de niños y adolescentes. Al principio, LADA está “enmascarada” y se clasifica inicialmente como diabetes tipo 2 porque el proceso de destrucción autoinmune de las células β en adultos puede ser más lento que en niños.
¡Atención!
Los síntomas de la enfermedad se borran, no hay polidipsia pronunciada, poliuria, pérdida de peso ni cetoacidosis. El exceso de peso corporal tampoco excluye la posibilidad de desarrollar LADA. La función de las células β disminuye lentamente, a veces durante varios años, lo que previene el desarrollo de cetoacidosis y explica la compensación satisfactoria del metabolismo de los carbohidratos cuando se toma PSSP en los primeros años de la enfermedad.
En tales casos, se diagnostica erróneamente diabetes tipo 2. La naturaleza gradual del desarrollo de la enfermedad conduce al hecho de que los pacientes buscan ayuda médica demasiado tarde, logrando adaptarse a la descompensación en desarrollo del metabolismo de los carbohidratos. En algunos casos, los pacientes acuden al médico entre 1 y 1,5 años después de la manifestación de la enfermedad. En este caso, se revelan todos los signos de una deficiencia aguda de insulina: bajo peso corporal, glucemia alta, falta de efecto del PSSP.
P. Z. Zimmet (1999) dio la siguiente definición de este subtipo de diabetes tipo 1: “La diabetes autoinmune que se desarrolla en adultos puede no ser clínicamente diferente de la diabetes tipo 2 y se manifiesta por un lento deterioro del control metabólico con el posterior desarrollo de insulina. dependencia." Al mismo tiempo, la presencia en pacientes de los principales marcadores inmunológicos de la diabetes tipo 1: autoanticuerpos contra antígenos de células β, junto con niveles bajos de péptido C basal y estimulado, permite diagnosticar una diabetes autoinmune de progresión lenta en adultos.
Principales criterios diagnósticos de LADA:
- presencia de autoanticuerpos contra GAD y/o ICA;
- niveles bajos de péptido C basal y estimulado;
- Presencia de alelos HLA de alto riesgo para diabetes tipo 1.
La presencia de autoanticuerpos contra antígenos de células β en pacientes con un cuadro clínico de diabetes tipo II al inicio de la enfermedad tiene un alto valor pronóstico en cuanto al desarrollo de la necesidad de insulina. Los resultados del Estudio Prospectivo de Diabetes del Reino Unido (UKPDS), que examinó a 3672 pacientes con un diagnóstico inicial de diabetes tipo 2, mostraron que los anticuerpos contra ICA y GAD tienen el mayor valor pronóstico en pacientes jóvenes ().
Según P. Zimmet, la prevalencia de LADA es de aproximadamente el 10-15% entre todos los pacientes con diabetes mellitus y aproximadamente el 50% de los casos ocurren en diabetes tipo 2 sin obesidad.
Los resultados de nuestro estudio mostraron que los pacientes de 30 a 64 años, que al inicio de la enfermedad presentaban un cuadro clínico de diabetes tipo 2 sin obesidad, disminución significativa del peso corporal (15,5 ± 9,1 kg) y enfermedades tiroideas autoinmunes concomitantes ( TDD) o AIT) representan un grupo con mayor riesgo de desarrollar LADA.
La determinación de autoanticuerpos contra GAD, ICA e insulina en esta categoría de pacientes es necesaria para el diagnóstico oportuno de LADA. Con mayor frecuencia en LADA se detectan anticuerpos contra GAD (según nuestros datos, en el 65,1% de los pacientes con LADA), en comparación con los anticuerpos contra ICA (en el 23,3% de los LADA) y contra la insulina (en el 4,6% de los pacientes). La presencia de una combinación de anticuerpos no es típica. El título de anticuerpos contra GAD en pacientes con LADA es menor que en pacientes con diabetes tipo 1 con la misma duración de la enfermedad.
Los pacientes con LADA representan un grupo de alto riesgo de desarrollar necesidades de insulina y requieren la administración oportuna de terapia con insulina. Los resultados de OGTT indican la ausencia de secreción de insulina estimulada en el 46% de los pacientes con LADA y su disminución en el 30,7% de los pacientes ya en los primeros 5 años de la enfermedad.
La ausencia de obesidad, la descompensación del metabolismo de los carbohidratos al tomar PSSP, los niveles basales bajos de insulina y péptido C en pacientes con LADA indican una alta probabilidad de ausencia de secreción de insulina estimulada y la necesidad de administración de insulina.
Si los pacientes con LADA tienen un alto grado de resistencia a la insulina e hipersecreción de insulina en los primeros años de la enfermedad, se recomienda prescribir medicamentos que no agoten la función de las células β, pero que mejoren la sensibilidad periférica de los tejidos a la insulina, por ejemplo. ejemplo biguanidas o glitazonas (actos, avandia). Estos pacientes suelen tener sobrepeso y una compensación satisfactoria del metabolismo de los carbohidratos, pero requieren mayor observación.
Para evaluar la resistencia a la insulina periférica se puede utilizar el índice de resistencia a la insulina - Homa-IR = ins0/22,5 eLnglu0 (donde ins0 es el nivel de insulina en ayunas y glu0 es la glucosa plasmática en ayunas) y/o el índice de sensibilidad tisular general a la insulina (ISI - índice de sensibilidad a la insulina, o índice de Matsuda*), obtenido en base a los resultados de la OGTT.
Con tolerancia normal a la glucosa, el Homa-IR es de 1,21 a 1,45 puntos; en pacientes con diabetes tipo 2, el valor de Homa-IR aumenta a 6 e incluso 12 puntos. El índice de Matsuda en el grupo con tolerancia normal a la glucosa es 7,3±0,1 UL–1 x ml x mg–1 x ml, y en presencia de resistencia a la insulina sus valores disminuyen.
Preservar la propia secreción de insulina residual en pacientes con diabetes mellitus tipo 1 es muy importante, ya que se observa que en estos casos la enfermedad es más estable y las complicaciones crónicas se desarrollan más lentamente y más tarde.
Se discute la cuestión de la importancia del péptido C en el desarrollo de complicaciones tardías de la diabetes mellitus. En el experimento se descubrió que el péptido C mejora la función renal y la utilización de la glucosa. Se descubrió que la infusión de pequeñas dosis de péptido C biosintético puede afectar la microcirculación en el tejido muscular humano y la función renal.
Para determinar LADA, están indicados estudios inmunológicos más extendidos entre pacientes con diabetes tipo 1, especialmente en ausencia de obesidad e ineficacia temprana del PSSP. El principal método de diagnóstico es la determinación de autoanticuerpos contra GAD y ICA.
Un grupo especial de pacientes que también requieren mucha atención y en los que es necesario determinar autoanticuerpos contra GAD e ICA son las mujeres con diabetes mellitus gestacional (DMG). Se ha establecido que el 2% de las mujeres con diabetes mellitus gestacional desarrollan diabetes tipo 1 en un plazo de 15 años.
Los mecanismos etiopatogenéticos del desarrollo de la DMG son muy heterogéneos, y para el médico siempre surge un dilema: ¿es la DMG la manifestación inicial de la diabetes tipo 1 o tipo 2? McEvoy et al. publicaron datos sobre la alta incidencia de autoanticuerpos contra ICA entre mujeres nativas y afroamericanas en Estados Unidos. Según otros datos, la prevalencia de autoanticuerpos contra ICA y GAD fue del 2,9 y el 5%, respectivamente, entre las mujeres finlandesas con antecedentes de DMG.
Por tanto, los pacientes con DMG pueden experimentar un desarrollo lento de diabetes mellitus insulinodependiente, como ocurre con la diabetes LADA. El cribado de pacientes con DMG para determinar autoanticuerpos contra GAD e ICA permite identificar pacientes que requieren administración de insulina, lo que permitirá lograr una compensación óptima del metabolismo de los carbohidratos.
Teniendo en cuenta los mecanismos etiopatogenéticos del desarrollo de LADA, la necesidad de terapia con insulina en estos pacientes se vuelve obvia, mientras que la terapia temprana con insulina tiene como objetivo no solo compensar el metabolismo de los carbohidratos, sino que también permite mantener la secreción de insulina basal en un nivel satisfactorio durante un largo tiempo. período.
El uso de derivados de sulfonilurea en pacientes con LADA implica una mayor carga sobre las células β y su agotamiento más rápido, mientras que el tratamiento debe tener como objetivo mantener la secreción de insulina residual y atenuar la destrucción autoinmune de las células β. En este sentido, el uso de secretogenos en pacientes con LADA es patogenéticamente injustificado.
¡Atención!
Después de la manifestación clínica, la mayoría de los pacientes con un cuadro clínico típico de diabetes tipo 1 experimentan en un período de 1 a 6 meses una disminución transitoria de las necesidades de insulina asociada con una mejora en la función de las células β restantes. Este es el período de remisión clínica de la enfermedad, o “luna de miel”.
La necesidad de insulina exógena se reduce significativamente (menos de 0,4 unidades/kg de peso corporal, en casos raros, incluso es posible una retirada completa de la insulina); El desarrollo de la remisión es una característica distintiva del inicio de la diabetes tipo 1 y ocurre en 18 a 62% de los casos de diabetes tipo 1 recién diagnosticada. La duración de la remisión varía de varios meses a 3 a 4 años.
A medida que avanza la enfermedad, la necesidad de exógenos aumenta y alcanza un promedio de 0,7 a 0,8 UI/kg de peso corporal. Durante la pubertad, la necesidad de insulina puede aumentar significativamente, hasta 1,0-2,0 U/kg de peso corporal. Con el aumento de la duración de la enfermedad debido a la hiperglucemia crónica, se desarrollan complicaciones micro (retinopatía, nefropatía, polineuropatía) y macrovasculares de la diabetes mellitus (daño a los vasos coronarios, cerebrales y periféricos). La principal causa de muerte es la insuficiencia renal y las complicaciones de la aterosclerosis.
Tratamiento
El objetivo del tratamiento de la diabetes tipo 1 es alcanzar los valores objetivo de glucemia, presión arterial y niveles de lípidos en sangre (), que pueden reducir significativamente el riesgo de desarrollar complicaciones micro y marcovasculares y mejorar la calidad de vida de los pacientes.
Los resultados del ensayo multicéntrico aleatorizado Diabetes Control and Complication Trail (DCCT) han demostrado de manera convincente que un buen control glucémico reduce la incidencia de complicaciones de la diabetes. Así, una disminución de la glucohemoglobina (HbA1c) del 9 al 7% condujo a una reducción del riesgo de desarrollar retinopatía diabética en un 76%, neuropatía en un 60% y microalbuminuria en un 54%.
El tratamiento de la diabetes tipo 1 incluye tres componentes principales:
- dietoterapia;
- ejercicio físico;
- terapia con insulina;
- entrenamiento y autocontrol.
Dietoterapia y actividad física.
En el tratamiento de la diabetes tipo 1, se deben excluir de la dieta diaria los alimentos que contengan carbohidratos de fácil digestión (azúcar, miel, dulces, bebidas dulces, mermeladas). Es necesario controlar el consumo (contar unidades de pan) de los siguientes productos: cereales, patatas, maíz, lácteos líquidos, frutas. La ingesta calórica diaria debe cubrirse entre un 55% y un 60% de carbohidratos, un 15-20% de proteínas y un 20-25% de grasas, mientras que la proporción de ácidos grasos saturados no debe superar el 10%.
El régimen de actividad física debe ser puramente individual. Cabe recordar que el ejercicio físico aumenta la sensibilidad de los tejidos a la insulina, reduce los niveles de glucemia y puede provocar el desarrollo de hipoglucemia. El riesgo de hipoglucemia aumenta durante el ejercicio y durante 12 a 40 horas después de un ejercicio extenuante prolongado.
El ejercicio de ligero a moderado que no dure más de 1 hora requiere una ingesta adicional de carbohidratos de fácil digestión antes y después del ejercicio. Con actividad física moderada, prolongada (más de 1 hora) e intensa, es necesario ajustar las dosis de insulina. Es necesario medir los niveles de glucosa en sangre antes, durante y después del ejercicio.
La terapia de reemplazo de insulina de por vida es esencial para la supervivencia de los pacientes con diabetes tipo 1 y desempeña un papel crucial en el tratamiento rutinario de esta enfermedad. Al prescribir insulina, se pueden utilizar diferentes regímenes. Actualmente, se acostumbra distinguir entre regímenes de terapia con insulina tradicional e intensificada.
La característica principal del régimen tradicional de terapia con insulina es la falta de ajuste flexible de la dosis de insulina administrada al nivel glucémico. En este caso, el autocontrol de la glucosa en sangre suele estar ausente.
Los resultados del DCCT multicéntrico demostraron de manera convincente la ventaja de la terapia intensificada con insulina para compensar el metabolismo de los carbohidratos en la diabetes tipo 1. La terapia intensiva con insulina incluye lo siguiente:
- principio de bolo basal de la terapia con insulina (inyecciones múltiples);
- número previsto de unidades de pan para cada comida (liberalización de la dieta);
- autocontrol (control de la glucosa en sangre durante todo el día).
Para el tratamiento de la diabetes tipo 1 y la prevención de complicaciones vasculares, los fármacos de elección son las insulinas humanas genéticamente modificadas. Las insulinas semisintéticas porcinas y humanas obtenidas de la carne de cerdo son de menor calidad en comparación con las humanas genéticamente modificadas.
La realización de terapia con insulina en esta etapa implica el uso de insulinas con diferentes duraciones de acción. Para crear un nivel básico de insulina, se utilizan insulinas de acción intermedia o de acción prolongada (aproximadamente 1 unidad por hora, que es un promedio de 24 a 26 unidades por día). Para regular el nivel de glucemia después de las comidas, se utilizan insulinas de acción corta o ultracorta en una dosis de 1-2 unidades por 1 unidad de pan.
Las insulinas de acción ultracorta (humalog, novorapid), así como las insulinas de acción prolongada (lantus), son análogos de la insulina. Los análogos de la insulina son polipéptidos especialmente sintetizados que tienen la actividad biológica de la insulina y una serie de propiedades específicas.
Estos son los preparados de insulina más prometedores en términos de terapia intensificada con insulina. Los análogos de la insulina Humalog (lispro, Lilly), así como novorapid (aspart, Novo Nordisk) son muy eficaces para regular la glucemia posprandial.
Su uso también reduce el riesgo de hipoglucemia entre comidas. Lantus (insulina glargina, Aventis) se produce mediante tecnología de ADN recombinante utilizando una cepa de laboratorio no patógena de Escherichia coli (K12) como organismo productor y se diferencia de la insulina humana en que el aminoácido asparagina de la posición A21 se reemplaza por glicina y 2 Se añaden moléculas de arginina en el extremo C de la cadena B. Estos cambios permitieron obtener un perfil de concentración constante y libre de picos de acción de la insulina durante las 24 horas del día.
Se han creado mezclas preparadas de insulinas humanas de diversas acciones, como Mixtard (30/70), Insuman Comb (25/75, 30/70), etc., que son mezclas estables de insulina de acción corta y prolongada. en proporciones especificadas.
Para la administración de insulina se utilizan jeringas de insulina desechables (U-100 para administrar insulina con una concentración de 100 U/ml y U-40 para insulina con una concentración de 40 U/ml), plumas de jeringa (Novopen, Humapen, Optipen, Bd -pen, Plivapen) y bombas de insulina. Se deben proporcionar jeringas a todos los niños y adolescentes con diabetes tipo 1, así como a las mujeres embarazadas con diabetes, a los pacientes con problemas de visión y a los amputados de miembros inferiores debido a la diabetes.
Alcanzar los valores glucémicos objetivo es imposible sin un autocontrol regular y un ajuste de las dosis de insulina. Los pacientes con diabetes tipo 1 deben controlar de forma independiente la glucemia diariamente, varias veces al día, para lo cual no solo se pueden usar glucómetros, sino también tiras reactivas para la determinación visual del azúcar en sangre (Glucocromo D, Betachek, Suprima Plus).
Para reducir la incidencia de complicaciones micro y macrovasculares de la diabetes, es importante alcanzar y mantener niveles normales de metabolismo de los lípidos y presión arterial.
Fuente: https://www.lvrach.ru/2005/05/4532521/
Diabetes tipo 1 y herencia
¡Saludos! Si recuerda el día en que a usted o a su hijo le diagnosticaron diabetes, también recordará las preguntas que comenzaron a preocupar a su cerebro febril. Me atrevo a suponer que nunca recibió respuesta a la pregunta: “¿De dónde vino la diabetes mellitus tipo 1 si no había nadie en su familia con esta enfermedad?”, al igual que a la pregunta: “¿La diabetes mellitus tipo 1 heredado y/o qué pasará con el resto de los hijos y familiares?” Probablemente todavía te molesten hasta el día de hoy.
Hoy intentaré responder a estas preguntas. La diabetes tipo 1 es una enfermedad multifactorial y poligénica. Nunca se puede decir qué factor es el principal o el principal. Algunos científicos dividen la diabetes tipo 1 en subtipos: A y B. Por cierto, la diabetes tipo 1 no es la única forma que puede ocurrir en la generación más joven.
El subtipo A se asocia con daño autoinmune al páncreas y la detección de anticuerpos lo confirma. Este subtipo se detecta con mayor frecuencia en niños y adolescentes. Pero sucede que no se detectan anticuerpos, pero la diabetes está presente. En este caso estamos hablando del subtipo B, que se presenta por motivos completamente diferentes y no relacionados con el funcionamiento del sistema inmunológico. Hasta la fecha estas causas se desconocen, por lo que la diabetes se denomina idiopática.
Investigación genética
Una cosa está clara: el tipo 1 es una enfermedad con predisposición hereditaria. ¿Qué significa esto y en qué se diferencia de una simple enfermedad hereditaria? El hecho es que una enfermedad hereditaria es la transmisión de un gen de generación en generación o una mutación de un gen en un organismo futuro. En este caso, ya nace una nueva persona con una patología o algún otro defecto.
En el caso de la diabetes todo es más complicado. Hay ciertos genes y secciones genéticas (hablaré en términos simplificados) que, cuando se combinan de cierta manera durante el encuentro del óvulo y el espermatozoide, aumentan el riesgo de desarrollar diabetes tipo 1. En otras palabras, no se hereda el gen defectuoso, sino el grado de riesgo de padecer la enfermedad.
Y para que la enfermedad se materialice, es decir, se desarrolle, son necesarios factores provocadores y un alto grado de riesgo. Si realizas un estudio genético, podrás identificar un cierto grado de riesgo, que puede ser alto, medio y bajo. Por lo tanto, no es en absoluto necesario que si una persona tiene riesgo de desarrollar diabetes tipo 1, la contraiga. Muy a menudo, el desarrollo de diabetes se asocia con los siguientes genes o regiones genéticas: HLA DR3, DR4 y DQ.
En este sentido, no importa en absoluto si usted no tiene antecedentes conocidos de diabetes tipo 1 en su familia ahora o en generaciones pasadas. Es muy posible que sus antepasados tuvieran un riesgo bajo que nunca se materializó. Y además de esto, ¿qué tan bien conoces tu árbol genealógico? ¿De qué morían los niños y los adultos a una edad temprana? Después de todo, los diagnósticos de hace 100 años no eran los más progresistas y no se consultaba con frecuencia a los médicos, especialmente en las zonas rurales.
Por tanto, creo que es completamente inútil buscar a los responsables de la propagación de la diabetes. Además, no debes reprocharte (me dirijo a los padres) por extrañar, no mirar y no salvar al niño. Para aliviar su culpa, le diré que el proceso autoinmune ocurre mucho antes de las manifestaciones clínicas de la diabetes, aproximadamente varios años y, en algunos casos, diez años.
Desde entonces, ha corrido mucha agua bajo el puente y es difícil recordar quién tiene la culpa de qué. Al final, por mucho que queramos, no podemos protegernos ni a nosotros ni a nuestros hijos de todo lo malo. Suceden cosas malas y si esto sucedió, entonces pensemos que es el DESTINO, que no se deja engañar.
investigación inmune
Cuando en una familia hay un familiar con diabetes tipo 1, para predecir la incidencia de diabetes en otros miembros de la familia se utiliza no sólo el estudio genético, sino también la determinación de autoanticuerpos, es decir, anticuerpos que luchan contra los tejidos del propio cuerpo. Por ejemplo, si un niño mayor tiene diabetes tipo 1, es posible que los padres quieran realizar pruebas genéticas y de anticuerpos en el niño más pequeño para identificar los riesgos de diabetes porque los anticuerpos aparecen mucho antes de que el niño muestre signos de diabetes.
- Anticuerpos contra las células beta de los islotes - ICA (detectados en 60-80% de los casos). Cuando se combina con GAD, aumenta drásticamente el riesgo de desarrollar diabetes, pero de forma aislada el riesgo de diabetes es pequeño.
- anticuerpos antiinsulina - IAA (detectados en 30-60% de los casos) En forma aislada, tiene poco efecto sobre el desarrollo de diabetes, el riesgo aumenta en presencia de otros anticuerpos;
- Anticuerpos contra la glutamato descarboxilasa - GAD (detectados en el 80-95% de los casos) Aumenta el riesgo de desarrollar diabetes, incluso en forma aislada.
Pero aquí también todo es ambiguo. La detección de cualquier grupo de anticuerpos en un niño no significa en absoluto que desarrollará diabetes en el futuro. Esto sólo significa que este niño tiene un alto riesgo de desarrollar diabetes, que puede no materializarse. Y además, nadie está a salvo de un error de laboratorio, por lo que se recomienda volver a realizar las pruebas después de 1-2 meses.
Por lo tanto, no recomiendo realizar pruebas de anticuerpos en miembros sanos de la familia. EN MI HUMILDE OPINIÓN. ¿Qué puedes hacer si sabes que tienes anticuerpos? Por supuesto, puedes formar parte de grupos experimentales donde se prueban métodos para prevenir la diabetes en grupos de alto riesgo, pero ¿te gustaría someter a un niño aún sano a manipulaciones desconocidas? Personalmente no estoy preparado y vivimos lejos del centro del país.
Aparte de molestias innecesarias, estas acciones no aportan nada bueno. Las expectativas y pensamientos constantes pueden algún día hacerse realidad. Personalmente creo que nuestros pensamientos son materiales y todo lo que pensamos algún día se hará realidad. Por lo tanto, no es necesario pensar en lo malo, atraer solo pensamientos positivos de que todo estará bien y todos los demás miembros de la familia estarán sanos.
Lo único que se puede hacer es determinar periódicamente la glucosa en ayunas y/o la hemoglobina glucosilada para no pasar por alto la manifestación de la diabetes. Porque hasta el momento no existen métodos probados que prevengan al 100% el desarrollo de diabetes, y no los hay en absoluto.
Otra pregunta que concierne a todas las personas con diabetes tipo 1: “¿Cuáles son los riesgos de morbilidad en los niños cuyos padres tienen diabetes o si la familia ya tiene un niño con diabetes?” Recientemente se completó un estudio de 16 años que examinó el pronóstico de la enfermedad en las familias de los pacientes. Aquí están sus resultados.
El riesgo de desarrollar diabetes sin un familiar conocido con diabetes es sólo del 0,2 al 0,4%. Cuanto mayor sea el número de familiares con diabetes en una familia, mayor será el riesgo. El riesgo de desarrollar diabetes para los familiares de una persona con diabetes tipo 1 es en promedio del 5%. Si dos niños de una familia están enfermos, el riesgo para el tercero es del 9,5%.
Si dos padres están enfermos, el riesgo de que el niño desarrolle diabetes tipo 1 aumenta hasta el 34%. Además, el riesgo de desarrollar diabetes tipo 1 depende de la edad a la que se manifiesta la enfermedad en el paciente. Cuanto antes se enferme un niño de la familia, mayor será el riesgo de que sufra un segundo. Si la manifestación de la enfermedad ocurrió antes de los 20 años, entonces el riesgo para el segundo hijo es del 6,4%, y si la manifestación de la enfermedad es mayor de 20 años, el riesgo es del 1,2%.
Prevención
Pero, ¿qué se puede hacer para reducir la influencia de estos notorios factores que desencadenan el proceso autoinmune? Y aunque todo se reduce a "afortunado o desafortunado", aún puedes intentar influir en ellos tanto como sea posible. Aquí hay una lista de métodos para la prevención primaria de la diabetes tipo 1.
- Prevención de infecciones intrauterinas e infecciones virales de la madre durante el embarazo.
- Prevención de determinadas infecciones virales en niños y adolescentes, como rubéola, sarampión, paperas, enterovirus, varicela, gripe.
- Tratamiento oportuno de focos crónicos de infección (sinusitis, dientes cariados, etc.).
- Realización de vacunación oportuna, estrictamente de acuerdo con las normas y vacunas probadas.
- Excluir la proteína de la leche de vaca de la dieta de los lactantes.
- Lactancia materna de larga duración (mínimo 18 meses).
- Excluida la introducción de alimentos complementarios que contengan productos que contengan gluten menores de un año.
- Exclusión de la dieta de alimentos que contengan nitratos, conservantes y colorantes.
- Ingesta normal de vitamina D.
- Agregar suplementos de ácidos grasos Omega 3 a su dieta.
- Reducir el consumo de carbohidratos rápidos debido al estrés excesivo en el páncreas.
En conclusión, quiero decir. Todos somos diferentes, con distintos grados de ansiedad y “nos importa un carajo”. Por lo tanto, depende de usted decidir si diagnosticar diabetes a su hijo o ir usted mismo. Pregúntese: “¿Estás preparado para un resultado positivo? ¿Estás listo para descubrir que tu hijo corre el riesgo de desarrollar esta enfermedad y al mismo tiempo seguir viviendo en paz? En caso afirmativo, puede someterse a un examen genético e inmunológico completo.
Si tiene diabetes tipo 1, su páncreas no puede producir insulina. Esta hormona vital ayuda a las células de su cuerpo a convertir el azúcar en energía.
Sin él, el azúcar se acumula en la sangre y puede alcanzar niveles peligrosos. Para evitar complicaciones potencialmente mortales, las personas con diabetes tipo 1 deben tomar insulina durante toda su vida.

Los síntomas de la diabetes tipo 1 generalmente comienzan repentinamente y pueden incluir:
- Mayor sed de lo habitual;
- Boca seca;
- Olor afrutado en el aire exhalado;
- Aumento de la diuresis.
Síntomas posteriores

Si los niveles de azúcar en sangre permanecen altos, la diabetes tipo 1 a menudo resulta en:
- Pérdida de peso;
- Apetito incrementado;
- Falta de energía, somnolencia.

Muchas personas con diabetes tipo 1 desarrollan afecciones cutáneas problemáticas, que incluyen:
- Infecciones bacterianas;
- Infecciones por hongos;
- Picazón, piel seca, mala circulación.
Las niñas con diabetes tipo 1 tienen más probabilidades de sufrir infecciones por hongos genitales. Los bebés pueden desarrollar candidiasis, una forma grave de dermatitis del pañal causada por hongos. Puede propagarse fácilmente desde la zona del pañal hasta los muslos y el abdomen.
Complicaciones peligrosas

Si sus niveles de glucosa en sangre no están controlados, la diabetes tipo 1 puede provocar síntomas más graves, como:
- Entumecimiento u hormigueo en las piernas;
- Deterioro de la visión;
- Niveles bajos de glucosa en sangre (llamados hipoglucemia);
- Pérdida de consciencia.
Si sus niveles de azúcar en sangre son demasiado altos o demasiado bajos, puede desarrollar un coma diabético. Es posible que no tenga ninguna señal de advertencia antes de que esto suceda. En este caso, se requiere atención médica de emergencia.

Sin tratamiento, la diabetes tipo 1 priva a las células del azúcar que necesitan para obtener energía. En cambio, su cuerpo comienza a quemar grasa, lo que conduce a la formación y acumulación de cetonas en la sangre. Estos son ácidos que pueden envenenar su cuerpo.
Esto, y otros cambios en la sangre, pueden desencadenar una afección potencialmente mortal llamada cetoacidosis. Esta situación requiere atención médica rápida y urgente. Es posible que necesite ser ingresado en el hospital.
Comparación de diabetes mellitus tipo 1 y 2

- En la diabetes tipo 1, su sistema inmunológico destruye las células del páncreas que producen insulina.
- En la diabetes tipo 2, el páncreas no se ve afectado. Por lo general, produce suficiente insulina, pero el cuerpo no la utiliza adecuadamente.
Los síntomas de ambas formas son los mismos, pero tienden a desarrollarse más rápidamente en personas con diabetes tipo 1.
¿Cuáles son las causas de la diabetes tipo 1?

Los médicos no saben exactamente qué causa exactamente que su sistema inmunológico ataque al páncreas. Los científicos han descubierto 50 genes o secuencias genéticas que aumentan la probabilidad de desarrollar diabetes tipo 1.
Pero esto en sí mismo no significa que esto vaya a suceder. Algunos investigadores creen que los desencadenantes ambientales también desempeñan un papel importante. Estos factores pueden incluir un virus o cambios que ocurren en su cuerpo durante el embarazo.
¿Quién desarrolla diabetes tipo 1?

La diabetes tipo 1 puede aparecer en cualquier momento de la vida. Pero en la mayoría de los casos, esta enfermedad se diagnostica antes de los 19 años.
Afecta por igual a niños y niñas y es más común en personas de raza blanca que en otros grupos étnicos. Según la Organización Mundial de la Salud, la diabetes tipo 1 es poco común en las poblaciones africana, india y asiática.

Su médico controlará su nivel de azúcar en sangre en ayunas o puede realizarle una prueba aleatoria de azúcar en sangre. También puede solicitar una prueba de hemoglobina glicosilada, que mostrará sus valores promedio de glucosa en sangre durante los últimos 2 o 3 meses.
Las pruebas deben repetirse en dos días distintos. Una prueba de tolerancia a la glucosa más compleja también ayudará a su médico a hacer un diagnóstico.
Problemas a largo plazo

Tener niveles altos de glucosa en sangre durante mucho tiempo puede dañar muchos de los sistemas de su cuerpo. La diabetes tipo 1 también puede aumentar la probabilidad de desarrollar las siguientes enfermedades:
- Enfermedades cardíacas y accidentes cerebrovasculares;
- Insuficiencia renal;
- Ceguera y otros problemas de visión;
- Enfermedad de las encías y pérdida de las encías;
- Daño a los nervios de brazos, piernas y órganos.
Controle sus niveles de azúcar en sangre

El primer paso para prevenir el desarrollo de complicaciones es controlar sus niveles de glucosa en sangre, por ejemplo con un medidor de glucosa. Para hacer esto, debe pincharse el dedo, aplicar una gota de sangre en una tira reactiva e insertarla en el medidor. Los resultados le ayudarán a cumplir con su plan de tratamiento. Cuando los niveles de glucosa estén cerca de lo normal, tendrá más energía, menos problemas de piel y un menor riesgo de sufrir enfermedades cardíacas y daños renales.
¿Puede ayudar la monitorización continua de la glucosa?
Este dispositivo utiliza un sensor que mide los niveles de glucosa de su cuerpo cada 10 segundos. Envía información a un monitor del tamaño de un teléfono móvil que lleva consigo.

El sistema registra automáticamente valores medios durante un máximo de 72 horas. El dispositivo no está diseñado para controlar diariamente los niveles de azúcar ni para un uso independiente a largo plazo. No reemplaza una prueba de glucosa en sangre regular, pero se utiliza para determinar patrones en los niveles de glucosa en sangre.
Tratamiento con inyecciones de insulina.

Todo paciente con diabetes tipo 1 debe tomar insulina. La mayoría de las personas lo toman mediante inyección y necesitan varias inyecciones cada día. Su médico le indicará cómo ajustar su dosis según los resultados de su medidor de glucosa en sangre. El objetivo es mantener estos niveles dentro de los valores normales con la mayor frecuencia posible.

La hipoglucemia ocurre cuando la insulina reduce los niveles de glucosa en sangre a niveles peligrosos. Puede ser leve, moderado o grave. Las señales de peligro incluyen:
- Somnolencia intensa o bostezos;
- Incapacidad para hablar o pensar con claridad;
- Pérdida de coordinación muscular;
- Sudoración, temblores, palidez;
- Convulsiones;
- Pérdida de consciencia.

Lleve consigo en todo momento al menos 15 gramos de carbohidratos de fácil digestión. Elevarán rápidamente los niveles de glucosa en sangre para combatir la hipoglucemia.
Algunos ejemplos de ellos:
- Media taza de jugo de frutas o refresco no dietético;
- 1 taza de leche;
- 2 cucharadas de pasas;
- 3 tabletas de glucosa o 5 caramelos.
Si su nivel de azúcar en sangre sigue siendo demasiado bajo después de 15 minutos, coma otros 15 gramos de estos carbohidratos.
Si pierde el conocimiento, es posible que necesite ayuda de las personas que lo rodean. Use un brazalete médico que indique que tiene diabetes y un kit de jeringa de glucagón. Este medicamento se puede inyectar debajo de la piel. Dígales a sus amigos y familiares cómo reconocer los signos de hipoglucemia y enséñeles cómo aplicar la inyección.

Este dispositivo puede reducir las posibilidades de desarrollar hipoglucemia. Libera insulina las 24 horas del día a través de un pequeño tubo que se inserta en la piel. Ya no necesitas inyecciones. Una bomba de insulina puede ayudar a mantener estables sus niveles de azúcar en sangre y brindarle más libertad en sus elecciones dietéticas. Existen algunas desventajas, así que pregúntele a su médico si esta opción es adecuada para usted.
Lo más probable es que su médico le recomiende hacerse una prueba de hemoglobina glicosilada cada 3 a 6 meses.

Esto mostrará qué tan bien se han controlado sus niveles de azúcar en sangre durante los últimos 2 o 3 meses. Si los resultados de su prueba son malos, es posible que deba ajustar su dosis de insulina o modificar su dieta o actividad física.
Si las inyecciones de insulina no logran controlar su nivel de glucosa en sangre o si experimenta hipoglucemia con frecuencia, su médico puede sugerirle un trasplante de células de los islotes pancreáticos.

Se trata de una cirugía experimental en la que el cirujano trasplanta células sanas productoras de insulina de un donante al páncreas. Pero hay un inconveniente: es posible que los resultados sólo duren unos pocos años. Y deberá tomar medicamentos contra el rechazo, que pueden tener efectos secundarios graves.

Los investigadores continúan trabajando en un sistema llamado páncreas artificial. Es una combinación de una bomba de insulina y un control continuo de la glucosa, que está controlado por un complejo programa informático. El objetivo es que funcione como un páncreas real. Esto significa que regulará la cantidad de insulina liberada en respuesta al aumento o disminución de los niveles de glucosa en sangre. Las primeras investigaciones sugieren que un páncreas artificial puede mejorar el control del azúcar en sangre.
Haga ejercicio con precaución
Debes estar físicamente activo, pero ten cuidado al hacer ejercicio. Para evitar una caída repentina de los niveles de glucosa en sangre, su médico puede recomendarle
Antes de hacer ejercicio, debes hacer lo siguiente:
- Controle sus niveles de glucosa;
- Ajuste su dosis de insulina;
- Tomar un bocadillo.
Su médico también puede recomendarle que realice pruebas de cetonas en la orina, una señal de que sus niveles de glucosa en sangre son muy altos. Evite el ejercicio extenuante cuando tenga estas sustancias en la orina.

Existen muchos mitos sobre lo que las personas con diabetes pueden y no pueden comer. La realidad es que ningún alimento está completamente prohibido. Puede consumir dulces como parte de una dieta y un plan de tratamiento bien equilibrados. Es importante trabajar con su médico para equilibrar sus inyecciones de insulina, su dieta y su actividad física.

Informe a su médico que planea quedar embarazada. Si su diabetes no está bien controlada, puede causar complicaciones, incluidos defectos de nacimiento en el bebé. Un buen control de la glucosa en sangre antes de la concepción reduce las posibilidades de desarrollar estos problemas y reduce el riesgo de aborto espontáneo. Además, también se reducirá el riesgo de daños oculares y picos peligrosos de presión arterial.

Cuando a un niño se le diagnostica diabetes, esto afecta a toda la familia. Los padres deben ayudarlo a determinar los niveles de glucosa en sangre, planificar las comidas y ajustar la dosis de insulina. Esta condición requiere atención las 24 horas, por lo que también debes programar el tratamiento mientras asistes a la escuela. Descubra quién en la escuela de su hijo puede administrarle una inyección de insulina si es necesario.
Estimados visitantes del sitio web de Farmamir. Este artículo no constituye un consejo médico y no debe sustituir la consulta con un médico.